İlaç endüstrisi, hastalıkları tedavi etmek ve önlemek veya semptomları hafifletmek amacıyla hastalara (veya kendi kendine uygulanan) uygulanacak ilaç olarak kullanılmak üzere farmasötik ilaçları keşfeden, geliştiren, üreten ve pazarlayan bir tıp endüstrisidir.[1][2] İlaç şirketleri jenerik veya markalı ilaçlar ve tıbbi cihazlarla uğraşabilir. İlaçların patentlenmesi, test edilmesi, güvenliği, etkililiği, ilaç testi ve pazarlanmasını düzenleyen çeşitli yasa ve düzenlemelere tabidirler. Küresel ilaç pazarı, 2020'de 1.228,45 milyar dolar değerinde tedavi üretti ve yıllık bileşik büyüme oranı (CAGR) %1,8'lik bir gösterdi.[3]
Tarih
1800'lerin ortaları – 1945: Botanikten ilk sentetik uyuşturuculara
İlaç endüstrisinin modern dönemi, 1800'lerin ortalarında asmorfin ve kinin gibi botanik ilaçları dağıtma konusundaki geleneksel rollerinden toptan üretime ve uygulamalı araştırmalardan kaynaklanan keşiflerden genişleyen yerel eczacılarla başladı. Bitkilerden yapılan kasıtlı ilaç keşfi, 1803 ve 1805 yılları arasında, bu bileşiğe Yunan rüya tanrısı Morpheus'un adını veren Alman eczacı asistanı Friedrich Sertürner tarafından afyondan analjezik ve uykuya neden olan bir ajan olan morfinin izolasyonu ile başladı.[4]1880'lerin sonlarında, Alman boya üreticileri, katran ve diğer mineral kaynaklarından bireysel organik bileşiklerin saflaştırılmasını mükemmelleştirmiş ve ayrıca organik kimyasal sentezde ilkel yöntemler oluşturmuşlardı.[5]Sentetik kimyasal yöntemlerin geliştirilmesi, bilim adamlarının kimyasal maddelerin yapısını sistematik olarak değiştirmelerine izin verdi ve ortaya çıkan farmakoloji bilimindeki büyüme, bu yapısal değişikliklerin biyolojik etkilerini değerlendirme yeteneklerini genişletti.
Epinefrin, norepinefrin ve amfetamin
1890'lara gelindiğinde, adrenal ekstraktların birçok farklı doku tipi üzerindeki derin etkisi keşfedildi ve hem kimyasal sinyalleme mekanizmasını hem de bu gözlemleri yeni ilaçların geliştirilmesi için kullanma çabalarını aradı. Adrenal ekstrelerin kan basıncını yükseltme ve vazokonstriktif etkileri, hemostatik ajanlar ve şok tedavisi olarak cerrahlar için özellikle ilgi çekiciydi ve bir dizi şirket, aktif maddenin değişen saflıklarını içeren adrenal özlere dayalı ürünler geliştirdi. 1897'de Johns Hopkins Üniversitesi'nden John Abel, aktif prensibi saf olmayan bir halde sülfat tuzu olarak izole ettiği epinefrin olarak tanımladı. Endüstriyel kimyager Jōkichi Takamine daha sonra saf bir durumda epinefrin elde etmek için bir yöntem geliştirdi ve teknolojiyi Parke-Davis'e lisansladı. Parke-Davis, epinefrini Adrenalin ticari adı altında pazarladı. Enjekte edilen epinefrin, astım ataklarının akut tedavisi için özellikle etkili olduğu kanıtlandı ve 2011 yılına kadar Amerika Birleşik Devletleri'nde inhale bir versiyon satıldı (Primatene Mist).[6][7]1929'da epinefrin, burun tıkanıklığı tedavisinde kullanılmak üzere bir inhaler halinde formüle edilmiştir.
Oldukça etkili olmakla birlikte, enjeksiyon gereksinimi epinefrin kullanımını sınırlamıştır[açıklama gerekli] ve oral olarak aktif türevler aranmıştır. Yapısal olarak benzer bir bileşik olan efedrin, Ma Huang bitkisindeki Japon kimyagerler tarafından tanımlandı ve Eli Lilly tarafından astım için oral bir tedavi olarak pazarlandı. Henry Dale ve George Barger'ın Burroughs-Wellcome'daki çalışmalarının ardından akademik kimyager Gordon Alles, 1929'da amfetamin sentezledi ve astım hastalarında test etti. İlacın sadece mütevazı anti-astım etkileri olduğu kanıtlandı, ancak coşku ve çarpıntı hissi üretti. Amfetamin, Smith, Kline ve French tarafından Benzedrine Inhaler ticari adı altında bir nazal dekonjestan olarak geliştirilmiştir. Amfetamin sonunda narkolepsi, post-ensefalitik parkinsonizm ve depresyon ve diğer psikiyatrik endikasyonlarda ruh hali yükselmesi için geliştirildi. 1937'de bu kullanımlar için Amerikan Tabipler Birliği'nden Yeni ve Resmi Olmayan bir Çare olarak onay aldı.[8]ve 1960'larda trisiklik antidepresanların gelişmesine kadar depresyon için yaygın kullanımda kaldı.[7]
Barbitüratların keşfi ve geliştirilmesi

1903'te Hermann Emil Fischer ve Joseph von Mering, dietilmalonik asit, fosfor oksiklorür ve üre reaksiyonundan oluşan dietilbarbitürik asidin köpeklerde uykuya neden olduğunu keşfettiklerini açıkladılar. Keşif, 1904'ten itibaren bir uyku yardımı olarak bileşiği Veronal ticari adı altında pazarlayan Bayer pharmaceuticals'a patentlendi ve lisanslandı. Yapısal değişikliklerin potens ve etki süresi üzerindeki etkisinin sistematik araştırmaları, 1911'de Bayer'de fenobarbitalin keşfine ve 1912'de güçlü anti-epileptik aktivitesinin keşfine yol açtı. Fenobarbital, 1970'ler boyunca epilepsi tedavisinde en yaygın kullanılan ilaçlar arasındaydı ve 2014 itibariyle Dünya Sağlık Örgütleri'nin temel ilaçlar listesinde yer almaktadır.[9][10]1950'ler ve 1960'lar, barbitüratların ve amfetaminlerin bağımlılık yaratan özellikleri ve kötüye kullanım potansiyeli hakkında artan farkındalık gördü ve kullanımları üzerinde artan kısıtlamalara ve reçete yazanların hükümet gözetiminin artmasına yol açtı. Bugün amfetamin, epilepsi tedavisinde dikkat eksikliği bozukluğu ve fenobarbital tedavisinde kullanımla büyük ölçüde sınırlıdır.[11][12]
1958'de Leo Sternbach, ilk benzodiazepin olan klordiazepoksiti (Librium) keşfetti. Düzinelerce başka benzodiazepin geliştirildi ve kullanılıyor, daha popüler ilaçlardan bazıları diazepam (Valium),alprazolam (Xanax), klonazepam (Klonopin) ve lorazepam (Ativan). Çok daha üstün güvenlik ve terapötik özellikleri nedeniyle, benzodiazepinler, bazı özel durumlar dışında tıpta barbitüratların kullanımının yerini büyük ölçüde almıştır. Daha sonra barbitüratlar gibi benzodiazepinlerin etkinliklerini önemli ölçüde kaybettiği ve uzun süre alındığında ciddi yan etkileri olabileceği keşfedildiğinde, Heather Ashton benzodiazepin bağımlılığını araştırdı ve kullanımlarını bırakmak için bir protokol geliştirdi.
İnsülin
1800'lerin sonlarından 1900'lerin başlarına kadar yapılan bir dizi deney, diyabetin normalde pankreas tarafından üretilen bir maddenin olmamasından kaynaklandığını ortaya koydu. 1869'da Oskar Minkowski ve Joseph von Mering, pankreasın cerrahi olarak çıkarılmasıyla köpeklerde diyabetin indüklenebileceğini buldular. 1921'de Kanadalı profesör Frederick Banting ve öğrencisi Charles Best bu çalışmayı tekrarladı ve pankreas ekstraktı enjeksiyonlarının pankreas çıkarılmasıyla üretilen semptomları tersine çevirdiğini buldu. Kısa süre sonra, ekstraktın insanlarda çalıştığı gösterildi, ancak rutin bir tıbbi prosedür olarak insülin tedavisinin geliştirilmesi, materyali yeterli miktarda ve tekrarlanabilir saflıkta üretmedeki zorluklar nedeniyle ertelendi. Araştırmacılar, şirketin biyolojik malzemelerin büyük ölçekli saflaştırılması konusundaki deneyimine dayanarak Eli Lilly and Co.'daki endüstriyel işbirlikçilerden yardım istedi. Kimyager George B. Eli Lilly and Company'den Walden, ekstraktın pH'ının dikkatli bir şekilde ayarlanmasının nispeten saf bir insülin derecesinin üretilmesine izin verdiğini buldu. Toronto Üniversitesi'nin baskısı ve bağımsız olarak benzer bir saflaştırma yöntemi geliştiren akademik bilim adamlarının potansiyel bir patent zorluğu altında, birden fazla şirket tarafından münhasır olmayan insülin üretimi için bir anlaşmaya varıldı. İnsülin tedavisinin keşfinden ve yaygın mevcudiyetinden önce, şeker hastalarının yaşam beklentisi sadece birkaç aydı.[13]
Erken anti-enfektif araştırma: Salvarsan, Prontosil, Penisilin ve aşılar
Bulaşıcı hastalıkların tedavisi için ilaçların geliştirilmesi, erken araştırma ve geliştirme çabalarının ana odak noktasıydı; 1900'de zatürree, tüberküloz ve ishal, Amerika Birleşik Devletleri'nde önde gelen üç ölüm nedeniydi ve yaşamın ilk yılında ölüm oranı %10'u aştı.[14][15][başarısız doğrulama]
1911'de ilk sentetik anti-enfektif ilaç olan arsfenamin, Berlin'deki Deneysel Terapi Enstitüsü'nden Paul Ehrlich ve kimyager Alfred Bertheim tarafından geliştirildi. İlaca Salvarsan ticari adı verildi.[16]Ehrlich, hem arsenikin genel toksisitesine hem de belirli boyaların bakteriler tarafından seçici olarak emililmesine dikkat çekerek, benzer seçici emilim özelliklerine sahip bir arsenik içeren bir boyanın bakteriyel enfeksiyonları tedavi etmek için kullanılabileceğini varsaydı. Arsfenamin, bu tür bir dizi bileşiği sentezleme kampanyasının bir parçası olarak hazırlandı ve kısmen seçici toksisite sergilediği bulundu. Arsfenamin, daha sonra tedavi edilemez olan ve amansız bir şekilde ciddi cilt ülserasyonuna, nörolojik hasara ve ölüme yol açan bir hastalık olan frengi için ilk etkili tedavi olduğunu kanıtladı.[17]
Ehrlich'in sentetik bileşiklerin kimyasal yapısını sistematik olarak değiştirme ve bu değişikliklerin biyolojik aktivite üzerindeki etkilerini ölçme yaklaşımı, Bayer bilim adamları Josef Klarer, Fritz Mietzsch ve Gerhard Domagk da dahil olmak üzere sanayi bilimcileri tarafından geniş çapta takip edildi. Alman boya endüstrisinden elde edilen bileşiklerin test edilmesine de dayanan bu çalışma, antibiyotiklerin sülfonamid sınıfının ilk temsilcisi olan Prontosil'ingeliştirilmesine yol açtı. Arsfenamin ile karşılaştırıldığında, sülfonamidler daha geniş bir aktivite yelpazesine sahipti ve çok daha az toksikti, bu da onları streptokoklar gibi patojenlerin neden olduğu enfeksiyonlar için yararlı hale getirdi.[18]1939'da Domagk, bu keşfi için Nobel Tıp Ödülü'nü aldı.[19][20]Bununla birlikte, II. Dünya Savaşı'ndan önce meydana gelen bulaşıcı hastalıklardan ölümlerdeki çarpıcı düşüş, öncelikle temiz su ve daha az kalabalık konut gibi gelişmiş halk sağlığı önlemlerinin sonucuydu ve anti-enfektif ilaçların ve aşıların etkisi esas olarak II. Dünya Savaşı'ndan sonra önemliydi.[21][22]
1928'de Alexander Fleming, penisilinin antibakteriyel etkilerini keşfetti, ancak insan hastalığının tedavisi için sömürülmesi, büyük ölçekli üretimi ve saflaştırılması için yöntemlerin geliştirilmesini bekliyordu. Bunlar, dünya savaşı sırasında ABD ve İngiliz hükümeti liderliğindeki bir ilaç şirketleri konsorsiyumu tarafından geliştirildi.[23]
Bu dönem boyunca, öncelikle yaygın bulaşıcı hastalıklardan sorumlu patojenlerin tanımlanmasına yönelik akademik ve devlet tarafından finanse edilen temel araştırmalar şeklinde aşıların geliştirilmesine yönelik erken ilerleme kaydedildi. 1885'te Louis Pasteur ve Pierre Paul Émile Roux ilk kuduz aşısınıyarattı. İlk difteri aşıları 1914'te difteri toksini ve antitoksin (aşılanmış bir hayvanın serumundan üretilen) karışımından üretildi, ancak aşılamanın güvenliği marjinaldi ve yaygın olarak kullanılmadı. Amerika Birleşik Devletleri, 1921'de 206.000 difteri vakası kaydetti ve 15.520 ölümle sonuçlandı. 1923'te, Pasteur Enstitüsü'ndeki Gaston Ramon ve Wellcome Araştırma Laboratuvarları'ndaki (daha sonra GlaxoSmithKline'ın bir parçası) Alexander Glenny'ninparalel çabaları, difteri toksininin formaldehit ile tedavi edilmesiyle daha güvenli bir aşının üretilebileceğinin keşfine yol açtı.[24]1944'te Squibb Pharmaceuticals'dan Maurice Hilleman, Japon Ensefalitine karşı ilk aşıyı geliştirdi.[25]Hilleman daha sonra kızamık, kabakulak, suçiçeği, kızamıkçık, hepatit A, hepatit B ve menenjite karşı aşıların geliştirilmesinde kilit rol oynadığı Merck'e taşındı.
Güvenli olmayan ilaçlar ve erken endüstri düzenlemesi

20. yüzyıldan önce, ilaçlar genellikle üretim veya güvenlik ve etkinlik iddiaları üzerinde çok az düzenleyici kontrole sahip küçük ölçekli üreticiler tarafından üretiliyordu. Bu tür yasaların var olduğu ölçüde, uygulama gevşekti. Amerika Birleşik Devletleri'nde, aşıların ve diğer biyolojik ilaçların artan düzenlemesi, kontamine çiçek aşısı ve difteri antitoksininin dağıtımının neden olduğu tetanos salgınları ve ölümler tarafından teşvik edildi.[26]1902 tarihli Biyolojik Kontrol Yasası, federal hükümetin her biyolojik ilaç ve bu tür ilaçları üreten süreç ve tesis için pazar öncesi onay vermesini gerektirdi. Bunu 1906'da, karıştırılmış veya yanlış markalanmış gıda ve ilaçların eyaletler arası dağıtımını yasaklayan Saf Gıda ve İlaç Yasası izledi. Bir ilaç, alkol, morfin, afyon, kokain veya diğer potansiyel olarak tehlikeli veya bağımlılık yapan uyuşturuculardan herhangi birini içeriyorsa ve etiketi bu tür uyuşturucuların miktarını veya oranını göstermiyorsa yanlış markalı olarak kabul edildi. Hükümetin, desteklenmeyen etkinlik iddialarında bulundukları için üreticileri kovuşturmak için yasayı kullanma girişimleri, federal hükümetin uygulama yetkilerini ilacın bileşenlerinin yanlış spesifikasyonu vakalarıyla sınırlayan bir Yüksek Mahkeme kararıyla baltalandı.[27]
1937'de S.E. tarafından üretilen "Elixir Sulfanilamide"i yuttuktan sonra 100'den fazla kişi öldü. Tennessee Massengill Şirketi. Ürün, şu anda antifriz olarak yaygın olarak kullanılan oldukça toksik bir çözücü olan dietilen glikol içinde formüle edilmiştir.[28]O zamanlar mevcut olan yasalara göre, üreticinin kovuşturulması ancak ürünün kelimenin tam anlamıyla etanolde bir çözüm anlamına gelen "eliksir" olarak adlandırıldığı teknik olarak mümkündü. Bu bölüme yanıt olarak, ABD Kongre, ilk kez bir ilaç satılmadan önce piyasa öncesi güvenliğin gösterilmesini gerektiren ve yanlış terapötik iddiaları açıkça yasaklayan 1938 Federal Gıda, İlaç ve Kozmetik Yasasını kabul etti.[29]
Savaş sonrası yıllar, 1945–1970
Anti-enfektif araştırmalarda daha fazla ilerleme
İkinci Dünya Savaşı'nın ardından, yeni antibakteriyel ilaç sınıflarının keşfinde bir patlama görüldü.[30]sefalosporinler dahil (Giuseppe Brotzu ve Edward Abraham'ın çığır açan çalışmalarına dayanarak Eli Lilly tarafından geliştirilmiştir),[31][32] streptomisin (Selman Waksman'ın laboratuvarında Merck tarafından finanse edilen bir araştırma programı sırasında keşfedildi[33]), tetrasiklinler[34](şimdi Pfizer'ın bir parçası olan Lederle Laboratuvarlarında keşfedildi), eritromisin (Eli Lilly and Co.'da keşfedildi)[35]ve giderek daha geniş bir yelpazede bakteriyel patojenlere genişlemeleri. 1943'te Selman Waksman'ın Rutgers'daki laboratuvarında Merck tarafından finanse edilen bir araştırma programı sırasında keşfedilen Streptomisin, tüberküloz için ilk etkili tedavi oldu. Keşfedildiği sırada, tüberküloz bulaşmış insanların izolasyonu için sanitoryumlar, gelişmiş ülkelerdeki şehirlerin her yerde bulunan bir özelliğiydi ve %50'si kabulden sonraki 5 yıl içinde öldü.[33][36]
1958'de yayınlanan bir Federal Ticaret Komisyonu raporu, antibiyotik gelişiminin Amerikan halk sağlığı üzerindeki etkisini ölçmeye çalıştı. Raporda, 1946–1955 döneminde, antibiyotiklerin etkili olduğu hastalıkların görülme sıklığında %42, antibiyotiklerin etkili olmadığı hastalıklarda ise sadece %20 düşüş olduğu bulundu. Raporda, "antibiyotik kullanımı, erken tanı ve diğer faktörlerin salgının yayılmasını ve dolayısıyla ortaya çıkan bu hastalıkların sayısını sınırladığı görülüyor" sonucuna vardı. Çalışma, antibiyotiklerin etkili tedavi sunduğu sekiz yaygın hastalığın (frengi, tüberküloz, dizanteri, kızıl, boğmaca, meningokok enfeksiyonları ve zatürree) ölüm oranlarını daha ayrıntılı olarak inceledi ve aynı dönemde %56'lık bir düşüş buldu.[37]Bunlar arasında tüberküloza bağlı ölümlerde %75'lik bir düşüş dikkate değerdi.[38]
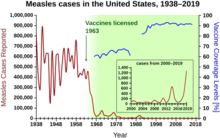
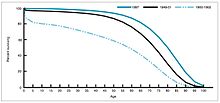
1940-1955 yılları arasında, ABD ölüm oranındaki düşüş oranı yılda %2'den yılda %8'e yükseldi, ardından yıllık %2'lik tarihsel orana geri döndü. Savaş sonrası yıllardaki dramatik düşüş, bu yıllarda meydana gelen bulaşıcı hastalıklar için yeni tedavilerin ve aşıların hızlı bir şekilde geliştirilmesine bağlandı.[40][22]Aşı geliştirme hızlanmaya devam etti ve dönemin en önemli başarısı, Jonas Salk'ın 1954'te kar amacı gütmeyen Ulusal İnfantil Felç Vakfı'nın finansmanı altında çocuk felci aşısını geliştirmesiydi. Aşı süreci hiçbir zaman patentli değildi, bunun yerine düşük maliyetli bir jenerik olarak üretmeleri için ilaç şirketlerine verildi. 1960 yılında Merck Sharp & Dohme'dan Maurice Hilleman, daha sonra birçok memeli türünde tümöre neden olduğu gösterilen SV40 virüsünü tanımladı. Daha sonra, SV40'ın Amerika Birleşik Devletleri'ndeki çocukların %90'ına uygulanan çocuk felci aşısı lotlarında bir kirletici olarak mevcut olduğu belirlendi.[41][42]Kontaminasyon hem orijinal hücre stoğunda hem de üretim için kullanılan maymun dokusundan kaynaklanmış gibi görünüyor. 2004 yılında Ulusal Kanser Enstitüsü, SV40'ın insanlarda kanserle ilişkili olmadığı sonucuna vardığını duyurdu.[43]
Dönemin diğer önemli yeni aşıları arasında kızamık için olanlar (1962, Boston Çocuk Tıp Merkezi'dan John Franklin Enders, daha sonra Merck'te Maurice Hilleman tarafından rafine edilmiş), Rubella (1969, Hilleman, Merck) ve kabakulak (1967, Hilleman, Merck)[44]Amerika Birleşik Devletleri'nde kızamıkçık, konjenital kızamıkçık sendromu, kızamık ve kabakulak insidansları, yaygın aşılamanın hemen ardından >%95 oranında düştü.[45]ABD'de lisanslı kızamık aşısının ilk 20 yılı, tahmini 52 milyon hastalık vakası, 17.400 zeka geriliği vakası ve 5.200 ölümü önledi.[46]
Antihipertansif ilaçların geliştirilmesi ve pazarlanması
Hipertansiyon ateroskleroz için bir risk faktörüdür,[47] kalp yetmezliği,[48] koroner arter hastalığı,[49][50] inme,[51] böbrek hastalığı,[52][53]ve periferik arter hastalığı,[54][55]ve sanayileşmiş ülkelerde kardiyovasküler morbidite ve mortalite için en önemli risk faktörüdür.[56]1940'tan önce, 50 yaşın üzerindeki kişiler arasındaki tüm ölümlerin yaklaşık %23'ü hipertansiyona bağlandı. Ağır hipertansiyon vakaları ameliyatla tedavi edildi.[57]
Hipertansiyon tedavisi alanındaki erken gelişmeler, kuaterner amonyum iyonu sempatik sinir sistemi bloke edici ajanları içeriyordu, ancak bu bileşikler ciddi yan etkileri nedeniyle hiçbir zaman yaygın olarak kullanılmadı, çünkü yüksek tansiyonun uzun vadeli sağlık sonuçları henüz belirlenmemişti ve enjeksiyonla uygulanmaları gerekiyordu.
1952'de Ciba'daki araştırmacılar, oral olarak mevcut ilk vazodilatör olan hidralazin'i keşfetti.[58]Hidralazin monoterapisinin önemli bir eksikliği, zamanla etkinliğini kaybetmesiydi (takifilaksi). 1950'lerin ortalarında Karl H. Beyer, James M. Sprague, John E. Baer ve Frederick C. Merck and Co.'dan Novello, günümüzde en yaygın kullanılan antihipertansif ilaç olmaya devam eden klorotiyazidi keşfetti ve geliştirdi.[59]Bu gelişme, hipertansiyonu olan kişiler arasında ölüm oranında önemli bir düşüşle ilişkiliydi.[60]Mucitler, 1975'te "anlatılmamış binlerce hayatın kurtarılması ve milyonlarca hipertansiyon kurbanının acılarının hafifletilmesi" nedeniyle bir Halk Sağlığı Lasker Ödülü ile tanındı.[61]
2009 Cochrane incelemesi, yüksek tansiyonlu kişilerde tiazid antihipertansif ilaçların ölüm (RR 0.89), inme (RR 0.63), koroner kalp hastalığı (RR 0.84) ve kardiyovasküler olaylar (RR 0.70) riskini azalttığı sonucuna varmıştır.[62]Sağlama yıllarında diğer antihipertansif ilaç sınıfları geliştirildi ve döngü diüretikleri de dahil olmak üzere kombinasyon tedavisinde geniş kabul gördü (Lasix/furosemid, Hoechst Pharmaceuticals, 1963),[63] beta blokerler (ICI Pharmaceuticals, 1964)[64] ACE inhibitörleri ve anjiyotensin reseptör blokerleri. ACE inhibitörleri, diyabetik hastalarda hipertansiyon olup olmadığına bakılmaksızın yeni başlangıçlı böbrek hastalığı [RR 0.71] ve ölüm [RR 0.84] riskini azaltır.[65]
Oral Kontraseptifler
İkinci Dünya Savaşı'ndan önce birçok ülkede doğum kontrolü yasaklanmıştı ve Amerika Birleşik Devletleri'nde doğum kontrol yöntemlerinin tartışılması bile bazen Comstock yasaları uyarınca kovuşturmaya yol açtı. Oral kontraseptiflerin gelişim tarihi bu nedenle doğum kontrol hareketine ve aktivistler Margaret Sanger, Mary Dennett ve Emma Goldman'ın çabalarına yakından bağlıdır. Gregory Pincus tarafından yapılan temel araştırmalara ve Carl Djerassi tarafından Syntex'te ve Frank Colton tarafından G.D.'de geliştirilen progesteron için sentetik yöntemlere dayanmaktadır. Searle & Co., ilk oral kontraseptif olan Enovid, G.D. tarafından geliştirilmiştir. Searle & Co. ve 1960 yılında FDA tarafından onaylanmıştır. Orijinal formülasyon, çok fazla dozda hormon içeriyordu ve ciddi yan etkilere neden oldu. Bununla birlikte, 1962'ye kadar 1,2 milyon Amerikalı kadın hap alıyordu ve 1965'te bu sayı 6,5 milyona yükseldi.[66][67][68][69]Uygun bir geçici kontraseptif biçiminin mevcudiyeti, kadınlara sunulan yaşam tarzı seçeneklerinin genişletilmesi, kadınların doğum kontrol uygulaması için erkeklere olan bağımlılığının azaltılması, evliliğin gecikmesini teşvik edilmesi ve evlilik öncesi birlikte yaşamanın artırılması da dahil olmak üzere sosyal adetlerde dramatik değişikliklere yol açtı.[70]
Talidomid ve Kefauver-Harris Değişiklikleri

ABD'de, 1959'da Tennessee Senatörü Estes Kefauver liderliğindeki Kongre duruşmalarından FD&C Yasası'nın revizyonları için bir baskı ortaya çıktı. Duruşmalar, reklam suistimalleri, uyuşturucuların şüpheli etkinliği ve endüstrinin daha fazla düzenlenmesine duyulan ihtiyaç da dahil olmak üzere çok çeşitli politika konularını kapsıyordu. Yeni mevzuat için ivme geçici olarak genişletilmiş tartışma altında işaretlenirken, daha kapsamlı düzenleme ihtiyacının altını çizen ve yeni yasaların geçirilmesi için itici güç sağlayan yeni bir trajedi ortaya çıktı.
12 Eylül 1960'ta, bir Amerikalı lisans sahibi olan William S. Cincinnati'deki Merrell Company, 1956'dan beri Avrupa'da pazarlanan bir yatıştırıcı olan Kevadon (thalidomid) için yeni bir ilaç başvurusu yaptı. Bileşiği gözden geçirmekten sorumlu FDA sağlık görevlisi Frances Kelsey, talidomidin güvenliğini destekleyen verilerin eksik olduğuna inanıyordu. Firma, ilacın ciddi konjenital anormalliklerle olan ilişkisi nedeniyle Alman pazarından çekildiği Kasım 1961'e kadar Kelsey ve FDA'ya başvuruyu onaylamaları için baskı yapmaya devam etti. Avrupa'da ve başka yerlerde birkaç bin yenidoğan, talidomidin teratojenik etkilerine maruz kaldı. FDA'nın onayı olmadan firma, Kevadon'u araştırma kullanımı kisvesi altında 1.000'den fazla doktora dağıttı. 624 hamile hasta da dahil olmak üzere bu "çalışma"da 20.000'den fazla Amerikalı talidomid aldı ve yaklaşık 17 bilinen yenidoğan ilacın etkilerine maruz kaldı.[alıntı gerekli]
Thalidomid trajedisi, Kefauver'in Kongre'de duran uyuşturucu düzenlemesini geliştirme tasarısını yeniden canlandırdı ve Kefauver-Harris Değişikliği 10 Ekim 1962'de yasa haline geldi. Üreticiler bundan böyle FDA'ya ilaçlarının ABD pazarına girmeden önce etkili ve güvenli olduğunu kanıtlamak zorunda kaldılar. FDA, reçeteli ilaçların reklamını düzenleme ve iyi üretim uygulamaları oluşturma yetkisi aldı. Yasa, 1938 ve 1962 yılları arasında tanıtılan tüm ilaçların etkili olmasını gerektiriyordu. Bir FDA - Ulusal Bilimler Akademisi işbirlikçi çalışması, bu ürünlerin yaklaşık yüzde 40'ının etkili olmadığını gösterdi. On yıl sonra over-the-counter ürünleriyle de benzer şekilde kapsamlı bir çalışma başladı.[71]
1970–1990'lar
Statinler
1971'de, ilaç şirketi Sankyo için çalışan Japon bir biyokimyacı olan Akira Endo, Penicillium citrinum mantarı tarafından üretilen bir molekül olan mevastatini (ML-236B), vücut tarafından kolesterol üretmek için kullanılan kritik bir enzim olan HMG-CoA redüktazın bir inhibitörü olarak tanımladı.Hayvan denemeleri, klinik çalışmalarda olduğu gibi çok iyi inhibitör etki gösterdi, ancak köpeklerde yapılan uzun-term bir çalışma, daha yüksek dozlarda toksik etkiler buldu ve sonuç olarak mevastatin'in insan kullanımı için çok toksik olduğuna inanıldı. Mevastatin, tümörlerin olumsuz etkileri, kas bozulması ve bazen laboratuvar köpeklerinde ölüm nedeniyle hiçbir zaman pazarlanmadı.
P. Baş bilim adamı ve daha sonra Merck & Co'nun CEO'su Roy Vagelos ilgilendi ve 1975'ten itibaren Japonya'ya birkaç gezi yaptı. 1978'de Merck, ilk olarak 1987'de Mevacor olarak pazarlanan Aspergillus terreus mantarından lovastatini (mevinolin, MK803) izole etmişti.[72][73][74]
Nisan 1994'te, Merck sponsorlu bir çalışmanın, İskandinav Simvastatin Survival Study'in sonuçları açıklandı. Araştırmacılar, daha sonra Merck tarafından Zocor olarak satılan simvastatini, yüksek kolesterol ve kalp hastalığı olan 4.444 hasta üzerinde test etti. Beş yıl sonra çalışma, hastaların kolesterollerinde %35'lik bir azalma gördüğü ve kalp krizi geçirme şanslarının %42 azaldığı sonucuna vardı.[75]1995'te Zocor ve Mevacor, Merck'e 1 milyar ABD dolarının üzerinde yaptı. Endo, 2006 Japonya Ödülü'ne ve 2008'de Lasker-DeBakey Klinik Tıbbi Araştırma Ödülü'ne layık görüldü. "Kolesterolü düşürmek" için yaptığı "yeni bir molekül sınıfına yönelik öncü araştırma" için,[Cümle parçası][76][77]
21. Yüzyıl
Birkaç on yıldan beri, biyolojiklerin küçük moleküllü tedavilere kıyasla önemi artmaktadır. Biyoteknoloji alt sektörü, hayvan sağlığı ve Çin ilaç sektörü de önemli ölçüde büyüdü. Örgütsel tarafta, büyük uluslararası ilaç şirketleri değer paylarında önemli bir düşüş yaşadı. Ayrıca, çekirdek jenerik sektör (patent dışı markaların ikameleri) rekabet nedeniyle değerlendi.[78]
Torreya, ilaç endüstrisinin Şubat 2021'e kadar 7,03 trilyon ABD doları piyasa değerine sahip olduğunu ve bunun 6,1 trilyon ABD dolarının halka açık şirketlerin değeri olduğunu tahmin etti. Küçük Moleküller modalitesi, 2003'teki %84,6'dan %58,2 değerleme payına sahipti. Biologics %14,5'ten %30,5'e yükseldi. Çin İlaçlarının değerleme payı, 2003'ten 2021'e kadar %1'den %12'ye yükseldi ve şu anda %7,7 ile 3. sırada yer alan İsviçre'yi solladı. Amerika Birleşik Devletleri, küresel değerlemenin %40'ı ile hala açık ara en değerli ilaç endüstrisine sahipti.[79]2023, çoğu küçük firma olsa da, küresel olarak 129 kamu biyoteknoloji firmasında en az 10.000 kişi için işten çıkarma yılıydı; bu, kısmen kötüleşen küresel finansal koşullar ve "genel yatırımcılar" tarafından yapılan yatırımlarda bir azalma nedeniyle 2022'ye göre indirimlerde önemli bir artıştı.[80]Özel firmalar ayrıca 2023'te risk sermayesi yatırımlarında önemli bir düşüş gördü ve 2021'de başlayan ve aynı zamanda ilk halka arzlarda bir azalmaya yol açan düşüş eğilimini sürdürdü.[80]
Birleşme ve Devralmaların Etkisi
2022 tarihli bir makale, tipik olarak ilaç M&A (birleşmeler ve satın almalar için) olarak adlandırılan "ilaç geliştirme işinde anlaşmalar bilimsel atılımlar kadar önemli olabilir" diyerek bu kavramı kısa ve öz bir şekilde ifade etti.[81]21. yüzyılın başlarındaki en etkili çözümlerden bazılarının, özellikle Keytruda ve Humira'ya dikkat çekerek, yalnızca M&A faaliyetleriyle mümkün olduğunu vurguladı.[81]
Araştırma ve geliştirme
İlaç keşfi, potansiyel ilaçların keşfedildiği veya tasarlandığı süreçtir. Geçmişte, çoğu ilaç ya aktif maddeyi geleneksel ilaçlardan izole ederek ya da tesadüfi keşifle keşfedildi. Modern biyoteknoloji genellikle bir hastalık durumu veya patojenle ilgili metabolik yolları anlamaya ve moleküler biyoloji veya biyokimya kullanarak bu yolları manipüle etmeye odaklanır. Çok sayıda erken-stage ilaç keşfi geleneksel olarak üniversiteler ve araştırma kurumları tarafından gerçekleştirilmiştir.
İlaç geliştirme, bir bileşikin ilaç olarak uygunluğunu sağlamak için potansiyel bir ilaç olarak tanımlanmasından sonra üstlenilen faaliyetleri ifade eder. İlaç geliştirmenin amaçları, uygun formülasyon ve dozlamanın yanı sıra güvenliliği belirlemektir. Bu alanlardaki araştırmalar genellikle in vitro çalışmaların, in vivo çalışmaların ve klinik çalışmaların bir kombinasyonunu içerir. Geç aşama geliştirmenin maliyeti, genellikle daha büyük ilaç şirketleri tarafından yapıldığı anlamına geliyor.[82]İlaç ve biyoteknoloji endüstrisi, net satışlarının %15'inden fazlasını Araştırma ve Geliştirme için harcıyor ve bu, diğer endüstrilerle karşılaştırıldığında açık ara en yüksek pay.[83]
Çoğu zaman, büyük çok uluslu şirketler, çok çeşitli ilaç keşfi ve geliştirme, üretim ve kalite kontrol, pazarlama, satış ve dağıtıma katılarak dikey entegrasyon sergilerler. Daha küçük kuruluşlar ise genellikle ilaç adaylarını keşfetmek veya formülasyonlar geliştirmek gibi belirli bir yöne odaklanır. Çoğu zaman, yeni müstern maddelerin potansiyelini keşfetmek için araştırma kuruluşları ve büyük ilaç şirketleri arasında işbirlikçi anlaşmalar oluşturulur. Daha yakın zamanlarda, çok uluslu şirketler ilaç geliştirmeyi yönetmek için sözleşmeli araştırma kuruluşlarına giderek daha fazla güveniyorlar.[84]
İnovasyonun maliyeti
İlaç keşfi ve geliştirme çok pahalıdır; insanlarda kullanım için araştırılan tüm bileşiklerin sadece küçük bir kısmı, çoğu ülkede, bu ülkelerde pazarlanmadan önce yeni ilaçları onaylamak zorunda olan hükümet tarafından atanan tıbbi kurumlar veya kurullar tarafından onaylanır. 2010 yılında 18 NME (Yeni Moleküler Varlıklar) ve FDA tarafından üç biyolojik veya toplam 21'i onaylandı, 2009'da 26'dan ve 2008'de 24'ten düştü. Öte yandan, 2007“de toplamda sadece 18, 2006”da 22 onay vardı. İlaç Değerlendirme ve Araştırma Merkezi, 2001 yılından bu yana yılda ortalama 22,9 onay almıştır.[85]Bu onay ancak klinik öncesi geliştirme ve klinik denemelere yapılan yoğun yatırımların yanı sıra devam eden güvenlik izleme taahhüdünden sonra gelir. Bu süreçte yarı yolda başarısız olan ilaçlar genellikle büyük maliyetlere neden olurken, karşılığında hiçbir gelir elde etmez. Bu başarısız ilaçların maliyeti dikkate alınırsa, başarılı bir yeni ilaç (yeni kimyasal varlık veya NCE) geliştirmenin maliyeti 1,3 milyar ABD doları olarak tahmin edilmiştir.[86](pazarlama giderleri hariç). Bununla birlikte, 2012 yılında Profesörler Light ve Lexchin, yeni ilaçlar için onay oranının on yıllardır nispeten istikrarlı bir ortalama 15 ila 25 olduğunu bildirdi.[87]
Endüstri çapında araştırma ve yatırım, 2009 yılında rekor 65,3 milyar dolara ulaştı.[88]ABD'de araştırmanın maliyeti 1995 ile 2010 yılları arasında yaklaşık 34,2 milyar dolar iken, gelirler daha hızlı arttı (gelirler o zaman 200,4 milyar dolar arttı).[87]
Danışmanlık firması Bain & Company tarafından yapılan bir araştırma, yeni bir ilacı (pazarlama ve diğer işletme giderlerini hesaba katan) keşfetme, geliştirme ve piyasaya sürme maliyetinin (başarısız olan potansiyel ilaçlarla birlikte) beş yıllık bir süre içinde 2003 yılında yaklaşık 1,7 milyar dolara yükseldiğini bildirdi.[89]Forbes'a göre, 2010 yılına kadar geliştirme maliyetleri ilaç başına 4 milyar ila 11 milyar dolar arasındaydı.[90]
Bu tahminlerden bazıları, gelirler gerçekleşmeden yıllar önce yatırım sermayesinin fırsat maliyetini de dikkate alır (bkz. Paranın zaman-değeri). İlaçların keşfi, geliştirilmesi ve onaylanması için gereken çok uzun süre nedeniyle, bu maliyetler toplam giderin neredeyse yarısı kadar birikebilir. İlaç endüstrisi değer zincirinin doğrudan bir sonucu, büyük farmasötik çok uluslu şirketlerin, temel araştırmalarla ilgili riskleri giderek daha fazla dış kaynak sağlama eğiliminde olmalarıdır; bu, biyoteknoloji şirketlerinin giderek daha önemli bir rol oynaması ve genel stratejilerin buna göre yeniden tanımlanmasıyla endüstri ekosistemini bir şekilde yeniden şekillendirir.[91]Mevcut bir etken maddenin (Line-extensions olarak da adlandırılır) yeniden formüle edilmesine dayananlar gibi bazı onaylı ilaçların geliştirilmesi çok daha ucuzdur.
Ürün onayı
Amerika Birleşik Devletleri'nde, yeni farmasötik ürünlerin Gıda ve İlaç İdaresi (FDA) tarafından hem güvenli hem de etkili olduğu için onaylanması gerekir. Bu süreç genellikle, insan denemelerine devam etmeyi desteklemek için yeterli klinik öncesi veri içeren bir Araştırma Yeni İlaç dosyasınınsunulmasını içerir. IND onayını takiben, giderek daha büyük insan klinik çalışmalarının üç aşaması yürütülebilir. Faz I genellikle sağlıklı gönüllüler kullanarak toksisiteyi inceler. Faz II, hastalarda farmakokinetik ve dozlamayı içerebilir ve Faz III, amaçlanan hasta popülasyonunda çok geniş bir etkinlik çalışmasıdır. Faz III testinin başarıyla tamamlanmasının ardından, FDA'ya Yeni İlaç Başvurusu sunulur. FDA verileri gözden geçirir ve ürünün pozitif bir fayda-risk değerlendirmesi olduğu görülürse, ürünü ABD'de pazarlamak için onay verilir.[92]
En büyük klinik çalışmaların bile nadir yan etkilerin prevalansını etkili bir şekilde tahmin edememesi nedeniyle, onay sonrası sürveyansın dördüncü aşaması da genellikle gereklidir. Pazarlama sonrası gözetim, pazarlamadan sonra bir ilacın güvenliğinin yakından izlenmesini sağlar. Bazı durumlarda, endikasyonunun belirli hasta gruplarıyla sınırlı olması gerekebilir ve diğerlerinde madde piyasadan tamamen çekilir.
FDA, Orange Book sitesinde onaylanmış ilaçlar hakkında bilgi sağlar.[93]
Birleşik Krallık'ta, İlaç ve Sağlık Ürünleri Düzenleme Kurumu, kullanım için ilaçları onaylar ve değerlendirir. Normalde İngiltere ve diğer Avrupa ülkelerinde bir onay, ABD'de bir onaydan daha geç gelir. Ardından, Ulusal Sağlık Hizmeti'nin (NHS) kullanımlarına izin verip vermeyeceğine ve nasıl izin vereceğine karar veren, İngiltere ve Galler için Ulusal Sağlık ve Bakım Mükemmelliği Enstitüsü'dür (NICE). İngiliz Ulusal Formülerliği, eczacılar ve klinisyenler için temel kılavuzdur.
ABD dışındaki birçok batı ülkesinde, yeni teknolojiler sağlanmadan önce maliyet etkinliği analizinin “dördüncü engeli” gelişti. Bu, söz konusu teknolojilerin “etkililik fiyat etiketine” (örneğin, QALY başına maliyet açısından) odaklanmaktadır. İngiltere ve Galler'de NICE, ilaçların ve teknolojilerin NHS tarafından sağlanıp sağlanmayacağına ve hangi koşullarda sağlanacağına karar verirken, İskoçya'daki İskoç İlaç Konsorsiyumu ve Avustralya'daki İlaç Faydaları Danışma Komitesi ile benzer düzenlemeler mevcuttur. Bir ürün, onaylanacaksa maliyet etkinliği eşiğini geçmelidir. Tedaviler “paranın değerini” ve topluma net bir faydayı temsil etmelidir.
Yetim ilaçlar
Birkaç büyük ilaç düzenleme bölgesinde bazı nadir hastalıklar ("yetim hastalıklar") için özel kurallar vardır. Örneğin, Amerika Birleşik Devletleri'nde 200.000'den az hastayı içeren hastalıklar veya belirli durumlarda daha büyük popülasyonlar Yetim İlaç Yasası'na tabidir.[94]Bu tür hastalıkları tedavi etmek için ilaçların tıbbi araştırma ve geliştirme finansal olarak dezavantajlı olduğundan, bunu yapan şirketler, ilacın patentler tarafından korunup korunmadığına bakılmaksızın, sınırlı bir süre (yedi yıl) için vergi indirimleri, ücret feragatleri ve bu ilaç üzerinde pazar münhasırlığı ile ödüllendirilir.
Küresel satışlar
| Şirket | İlaç geliri ($ milyon) |
|---|---|
| Pfizer |
100.330 |
| Johnson & Johnson |
94.940 |
| Roche |
66,260 |
| Merck & Co |
59.280 |
| Abbvie |
58,050 |
| Novartis |
50,540 |
| Bristol Myers Squibb |
46,160 |
| Sanofi |
45.220 |
| AstraZeneca |
44.350 |
| GSK |
36.150 |
| Takeda |
30.000 |
| Eli Lilly ve Şirketi |
28,550 |
| Gilead Bilimleri |
27,280 |
| Bayer |
26,640 |
| Amgen |
26.320 |
| Boehringer Ingelheim |
25.280 |
| Novo Nordisk |
25.000 |
| Moderna |
19,260 |
| Merck KGaA |
19,160 |
| BioNTech |
18.200 |
2011 yılında, Avrupa ve Kuzey Amerika'da büyüme biraz yavaşlasa bile, reçeteli ilaçlara yapılan küresel harcamalar 954 milyar doları aştı. Amerika Birleşik Devletleri, küresel ilaç pazarının üçte birinden fazlasını oluşturuyor ve yıllık satışlarda 340 milyar dolar, onu AB ve Japonya takip ediyor.[96]Çin, Rusya, Güney Kore ve Meksika gibi gelişmekte olan pazarlar bu pazarı geride bırakıp yüzde 81 büyüdü.[97][98]
2013'ün en çok satan ilk on ilacı toplamda 75,6 milyar dolarlık satışa ulaştı ve anti-inflamatuar ilaç Humira, 10,7 milyar dolarlık satışla dünya çapında en çok satan ilaç oldu. İkinci ve üçüncü en çok satanlar sırasıyla Enbrel ve Remicade oldu.[99]2013 yılında Amerika Birleşik Devletleri'nde en çok satan ilk üç ilaç Abilify (6,3 milyar dolar) Nexium (6 milyar dolar) ve Humira (5,4 milyar dolar) idi.[100]Şimdiye kadar en çok satan ilaç olan Lipitor, yılda ortalama 13 milyar dolar elde etti ve Pfizer'ın patenti Kasım 2011'de sona ermeden önce ömrü boyunca toplam 141 milyar dolar elde etti.
IMS Health, bazı patentlerin kaybına rağmen çoğu sektörde artan karlar ve ufukta yeni “gişe rekorları kıran” ilaçlar da dahil olmak üzere, 2007 yılında ilaç endüstrisinde beklenen eğilimlerin bir analizini yayınlamaktadır.[101]
Patentler ve jenerikler
Bir dizi hususa bağlı olarak, bir şirket, tipik olarak yaklaşık 20 yıl boyunca münhasırlık hakları veren ilaç veya ilacı üretme süreci için bir patent başvurusunda bulunabilir ve alabilir.[102]Bununla birlikte, ancak ortalama 10 ila 15 yıl süren titiz bir çalışma ve testten sonra, hükümet yetkilileri şirkete ilacı pazarlaması ve satması için izin verecektir.[103]Patent koruması, patent sahibinin, markalı ilaç için yüksek kar marjları yoluyla araştırma ve geliştirme maliyetlerini geri kazanmasını sağlar. İlacın patent korumasının süresi dolduğunda, jenerik bir ilaç genellikle rakip bir şirket tarafından geliştirilir ve satılır. Jeneriklerin geliştirilmesi ve onaylanması daha ucuzdur ve daha düşük bir fiyata satılmalarına izin verir. Genellikle markalı ilacın sahibi, jenerik pazarda bir başlangıç yapmak için patentin süresi dolmadan önce jenerik bir versiyon tanıtacaktır.[104]Bu nedenle, 1990'larda endüstrinin "altın dönemi" sırasında başlatılan ürünlerin patentinin sona ermesi ve şirketlerin kaybedilen gelirlerin yerini alacak kadar yeni gişe rekorları kıran ürünler geliştirmemesi nedeniyle yeniden yapılanma rutin hale geldi.[105]
Reçeteler
ABD'de, reçetelerin değeri 1995“ten 2005”e kadar olan dönemde yüzde 61'lik bir artışla yıllık 3,4 milyar arttı. Reçeteli ilaçların perakende satışları yüzde 250'yi 72 milyar dolardan 250 milyar dolara sırarken, reçetelerin ortalama fiyatı 30 dolardan 68 dolara iki kattan fazla arttı.[106]
Pazarlama
Reklam, sağlık dergilerinde ve daha ana akım medya rotaları aracılığıyla yaygındır. Bazı ülkelerde, özellikle ABD'de, doğrudan halka reklam vermelerine izin verilir. İlaç şirketleri genellikle doğrudan ve kişisel olarak doktorlara ve diğer sağlık hizmeti sağlayıcılarına pazarlamak için satış görevlileri (genellikle “ilaç temsilcileri” veya daha eski bir terim “detaylı erkekler” olarak adlandırılır) istihdam eder. Bazı ülkelerde, özellikle de ABD'de, ilaç şirketleri de politikacıları etkilemek için lobiciler kullanıyor. ABD'de reçeteli ilaçların pazarlanması, 1987 tarihli federal Reçeteli İlaç Pazarlama Yasası ile düzenlenir. İlaç pazarlama planı, ilaç birliğini ve onun öğelerini ve yönetimlerini mevcut sahnede ileriye götürecek harcama planlarını, kanallarını ve düşünceleri içerir.
Sağlık çalışanlarına
Bad Pharma kitabı ayrıca ilaç temsilcilerinin etkisini, hayalet yazarların ilaç şirketleri tarafından akademisyenlerin yayınlaması için makale yazmak için nasıl kullanıldığını, akademik dergilerin gerçekte ne kadar bağımsız olduğunu, ilaç şirketlerinin doktorların sürekli eğitimini nasıl finanse ettiğini ve hasta gruplarının genellikle endüstri tarafından nasıl finanse edildiğini tartışıyor.[107]
Doğrudan tüketici reklamcılığına
1980'lerden bu yana, tüketicilere reçeteli ilaçlar için yeni pazarlama yöntemleri önem kazandı. Doğrudan tüketiciye yönelik medya reklamları, FDA Tüketiciye Yönelik Yayın Reklamları Endüstri Rehberi'nde yasallaştırıldı.
Tartışmalar
İlaç pazarlaması ve lobicilik
Farmasötik pazarlama ve etki ile ilgili artan tartışmalar var. Sağlık profesyonellerine sürekli pazarlama 'hediyeleri' ve önyargılı bilgiler sağlanması da dahil olmak üzere ilaç temsilcileri aracılığıyla doktorlar ve diğer sağlık profesyonelleri üzerinde etki suçlamaları ve bulguları olmuştur;[108]dergilerde ve konferanslarda oldukça yaygın reklam; bağımsız sağlık kuruluşlarının ve sağlığın teşvik kampanyalarının finanse edilmesi; doktorlar ve politikacılar için lobicilik yapmak (ABD'deki diğer tüm endüstrilerden daha fazla[109]); tıp fakülteleri veya hemşire eğitimi sponsorluğu; müfredat üzerinde etkisi olan sürekli eğitim etkinliklerinin sponsorluğu;[110]ve tıbbi danışma kurullarında ücretli danışman olarak hekimleri işe almak.
No Free Lunch ve AllTrials gibi bazı savunuculuk grupları, ilaç pazarlamasının doktorlara etkisini eleştirdiler çünkü diğerleri hasta için daha ucuz veya daha iyi olsa bile doktorları pazarlanan ilaçları reçete etmeye önyargılı hale getirdiğini söylüyorlar.[111]
Hastalık mongering ile ilgili suçlamalar var[112](aşırı tıbbi) ilaçlar için pazarı genişletmek için. Bu konuda 2006 yılında Avustralya'da bir açılış konferansı düzenlendi.[113]2009 yılında, Hükümet tarafından finanse edilen Ulusal Reçeteleme Servisi, pratisyen hekimleri bağımsız ilaç analizi yöntemleri konusunda eğitmeyi amaçlayan "Kanıt Bulma - Aldatmaca Tanıma" programını başlattı.[114]
Meta-analizler, ilaç şirketleri tarafından desteklenen psikiyatrik çalışmaların olumlu sonuçlar bildirme olasılığının birkaç kat daha fazla olduğunu ve bir ilaç şirketi çalışanı dahil olursa etkinin daha da büyük olduğunu göstermiştir.[115][116][117]Etki, mücadele edilen tıp fakültelerinde doktor ve hemşirelerin eğitimine de genişledi.
Zihinsel Bozuklukların Tanısal ve İstatistik El Kitabının tasarımının ve kriterlerin genişletilmesinin, ilaç şirketinin psikiyatri üzerindeki etkisi tarafından yönlendirilen insan doğasının artan bir tıbbileştirilmesini veya "hastalık tacılığını" temsil ettiği iddia edilmiştir.[118]Doğrudan çıkar çatışması potansiyeli, kısmen DSM-IV psikiyatrik bozukluklarını seçen ve tanımlayan yazarların kabaca yarısının ilaç endüstrisi ile finansal ilişkileri olduğu veya daha önce olduğu için ortaya çıkmıştır.[119]
ABD'de, 2013'ten itibaren, Hekim Mali Şeffaflık Raporları (Güneş Yasası'nın bir parçası) kapsamında, Medicare ve Medicaid Hizmetleri Merkezleri, doktorlar ve hastanelerle olan finansal ilişkileri hakkında bilgi bildirmek için ilgili üreticilerden ve grup satın alma kuruluşlarından bilgi toplamak zorundadır. Veriler, Centers for Medicare & Medicaid Services web sitesinde kamuya açıklanmaktadır. Beklenti, doktorlar ve İlaç endüstrisi arasındaki ilişkinin tamamen şeffaf hale gelmesidir.[120]
OpenSecrets tarafından yürütülen bir raporda, 2017 yılında ilaç işi için bir miktar kapasitede çalışan 1.100'den fazla lobici vardı. 2017'nin ilk çeyreğinde, sağlık ürünleri ve ilaç endüstrisi, Amerika Birleşik Devletleri Kongresi üyelerinin lobiciliğine 78 milyon dolar harcadı.[121]
İlaç fiyatlandırması
İlaçların fiyatlandırılması sağlık sistemleri için büyük bir zorluk haline geliyor.[122]Batı Sağlık Politikası Merkezi tarafından Kasım 2020'de yapılan bir araştırma, ABD'de 1,1 milyondan fazla yaşlı vatandaşın Medicare programının önümüzdeki on yıl içinde erken ölmesi bekleniyor çünkü reçeteli ilaçlarını karşılayamayacaklar ve sağlık komplikasyonları nedeniyle önlenebilir tıbbi maliyetlere yılda 17,7 milyar dolar daha harcanmasını gerektirecekler.[123]
Düzenleyici sorunlar
Ben Goldacre, Birleşik Krallık'taki İlaç ve Sağlık Ürünleri Düzenleme Ajansı (MHRA) veya Amerika Birleşik Devletleri'ndeki Gıda ve İlaç İdaresi (FDA) gibi düzenleyicilerin, düzenleyici ile şirketler arasında dönen kapı değişimi ve düzenleyici ile şirket çalışanları arasındaki dostlukların gelişmesi nedeniyle halkın çıkarlarından ziyade ilaç şirketlerinin çıkarlarını ilerlettiğini savundu.[124]Düzenleyicilerin, yeni ilaçların halihazırda mevcut olana göre bir iyileştirme sunmasını ve hatta özellikle etkili olmalarını gerektirmediğini savunuyor.[124]
Diğerleri, aşırı düzenlemenin terapötik yeniliği bastırdığını ve düzenleyici tarafından gerekli klinik çalışmaların mevcut maliyetinin, insan hastalığının tedavisi için yeni genetik ve biyolojik bilgilerin tam olarak kullanılmasını önlediğini savundu. Başkanın Bilim ve Teknoloji Danışmanları Konseyi tarafından hazırlanan 2012 tarihli bir raporda, 1) FDA'nın hızlandırılmış onay süreçlerini kullanımını genişletmek, 2) dar tanımlanmış popülasyonlarda kullanılması amaçlanan ilaçlar için hızlandırılmış bir onay yolu oluşturmak ve 3) yeni, uyarlanabilir bir ilaç onay sürecinin fizibilitesini değerlendirmek için tasarlanmış pilot projeler üstlenmek de dahil olmak üzere yeni ilaç geliştirmeye yönelik düzenleyici yükleri azaltmak için birkaç önemli öneride bulundu.[125]
İlaç sahtekarlığı
|
|
Bu bölümdeki örnekler ve bakış açısı öncelikle Amerika Birleşik Devletleri ile ilgilidir ve konuya dünya çapında bir bakış açısını temsil etmemektedir. (Ağustos 2015)
|
İlaç sahtekarlığı, bir ilaç şirketine finansal kazanç getiren aldatmaları içerir. Bireyleri ve kamu ve özel sigortacıları etkiler. Birkaç farklı şema var[126]ilaç endüstrisine özel sağlık sistemini dolandırmak için kullanılırdı. Bunlar şunları içerir: İyi Üretim Uygulamaları (GMP) İhlalleri, Etiket Dışı Pazarlama, En İyi Fiyat Dolandırıcılığı, CME Dolandırıcılığı, Medicaid Fiyat Raporlaması ve Üretilen Bileşik İlaçlar.[127]Bu miktarın 2,5 milyar doları, 2010 mali yılında Yanlış İddialar Yasası davaları aracılığıyla geri kazanıldı. Dolandırıcılık vakalarına örnek olarak GlaxoSmithKline 3 milyar dolarlık uzlaşma, Pfizer 2,3 milyar dolarlık uzlaşma ve Merck & Co. 650 milyon dolarlık uzlaşma verilebilir. Dolandırıcılıktan kaynaklanan zararlar, en yaygın olarak bir kişiyi "ihbarcı" veya ilişkili (yasa) olduğu için ödüllendiren qui tam hükümleri kapsamında, Sahte İddialar Yasası kullanılarak telafi edilebilir.[128]
Atipik antipsikotikler satan her büyük şirket—Bristol-Myers Squibb, Eli Lilly and Company, Pfizer, AstraZeneca ve Johnson & Johnson—ya Sahte İddialar Yasası uyarınca son hükümet davalarını yüz milyonlarca dolar karşılığında çözdü ya da şu anda olası sağlık sahtekarlığı için soruşturma altında. Yasadışı pazarlama suçlamalarının ardından, yerleşimlerden ikisi 2009 yılında şirketlere şimdiye kadar verilen en büyük ceza para cezaları için kayıtlar kırdı. Biri Eli Lilly'nin antipsikotik Zyprexa'sını, diğeri ise artrit için kullanılan bir anti-inflamatuar ilaç olan Bextra'yı içeriyordu. Bextra davasında, hükümet ayrıca Pfizer'ı başka bir antipsikotik olan Geodon'u yasadışı olarak pazarlamakla suçladı; Pfizer, herhangi bir yanlışı kabul etmeden iddianın bu kısmını 301 milyon dolarlık bir şekilde çözdü.[129]
2 Temmuz 2012'de GlaxoSmithKline, cezai suçlamaları kabul etti ve ABD'deki en büyük sağlık sahtekarlığı davasının ve bir ilaç şirketi tarafından yapılan en büyük ödemenin 3 milyar dolarlık bir çözüme kavuşturulmasını kabul etti.[130]Anlaşma, şirketin reçeteli ilaçları yasadışı olarak tanıtması, güvenlik verilerini bildirmemesi,[131] doktorlara rüşvet vermek ve ruhsatlı olmadıkları kullanımlar için ilaçları teşvik etmek. İlgili ilaçlar, etiket dışı, kapsanmamış kullanımlar için Paxil, Wellbutrin, Advair, Lamictal ve Zofran'dı. Bunlar ve Imitrex, Lotronex, Flovent ve Valtrex ilaçları geri tepme planına dahil oldu.[132][133][134]
Aşağıda, 1991“den 2012”ye kadar ilaç firmalarıyla ulaşılan en büyük dört anlaşmanın bir listesi, toplam yerleşimin büyüklüğüne göre sıralanmıştır. İlaç endüstrisine yönelik yasal iddialar, Medicare ve Medicaid sahtekarlığı, etiket dışı promosyon ve yetersiz üretim uygulamaları dahil olmak üzere son yirmi yılda büyük ölçüde değişmiştir.[135][136]
| Şirket | Yerleşim | İhlal(lar) | Yıl | Ürün(ler) | İddiaya göre yasalar ihlal edildi (varsa) |
|---|---|---|---|---|---|
| GlaxoSmithKline[137] | 3 milyar dolar | Etiket dışı promosyon/ güvenlik verilerinin ifşa edilmemesi |
2012 | Avandia/Wellbutrin/Paxil | Yanlış İddialar Yasası/FDCA |
| Pfizer[138] | 2,3 milyar dolar | Etiket dışı promosyon/geri kopasma | 2009 | Bextra/Geodon/ Zyvox/Lyrica |
Yanlış İddialar Yasası/FDCA |
| Abbott Laboratuvarları[139] | 1,5 milyar dolar | Etiket dışı promosyon | 2012 | Depakote | Yanlış İddialar Yasası/FDCA |
| Eli Lilly[140] | 1,4 milyar dolar | Etiket dışı promosyon | 2009 | Zyprexa | Yanlış İddialar Yasası/FDCA |
Hekim rolleri
Mayıs 2015'te New England Journal of Medicine, yeni tedavilerin geliştirilmesi için ilaç endüstrisi-hekim etkileşimlerinin önemini vurguladı ve endüstrinin suihhimaline yönelik ahlaki öfkenin haksız bir şekilde birçok kişinin finansal çıkar çatışmalarının yarattığı sorunları aşırı vurgulamasına yol açtığını savundu. Makalede, Ulusal Sağlık Enstitüleri Ulusal Çeviri Bilimlerini Geliştirme Merkezi, Başkanın Bilim ve Teknoloji Danışmanları Konseyi, Dünya Ekonomik Forumu, Gates Vakfı, Wellcome Trust ve Gıda ve İlaç İdaresi gibi büyük sağlık kuruluşlarının, hastalara sağlanan faydaları iyileştirmek için doktorlar ve endüstri arasında daha fazla etkileşimi teşvik ettiğini belirtti.[141][142]
COVID-19'a yanıt
Kasım 2020'de birkaç ilaç şirketi, enfeksiyonu önlemede %90 ila 95'lik bir etkinlikle COVID-19 aşılarının başarılı denemelerini duyurdu. Dış analistler tarafından incelenen şirket duyuruları ve verileri başına göre, bu aşılar doz başına 3 ila 37 dolar olarak fiyatlandırılır.[143]Wall Street Journal, bu başarının Nobel Barış Ödülü ile tanınması çağrısında bulunan bir başyazı yayınladı.[144]
Sınır Tanımayan Doktorlar, ilaç, test ve aşılar üzerindeki yüksek fiyatların ve tekellerin pandemiyi uzatacağı ve hayatlara mal olacağı konusunda uyardı. Hükümetleri, Kanada, Şili, Ekvador, Almanya ve İsrail tarafından daha önce yapıldığı gibi, gerektiğinde zorunlu lisansları kullanarak vurgunculuk yapmayı önlemeye çağırdılar.[145]
20 Şubat'ta 46 ABD'li milletvekili, ABD hükümetine, özel üreticilere fiyat ve bulunabilirlik üzerinde özel kontrol vermekten kaçınmak için herhangi bir koronavirüs aşısı ve tedavisi için vergi mükelleflerine geliştirme parası verirken tekel hakları vermemesi çağrısında bulundu.[146]
Amerika Birleşik Devletleri'nde hükümet, potansiyel COVID-19 terapötikleri için araştırma ve geliştirme ve/veya üretim tesislerinin inşasının sübvanse edildiği anlaşmalar imzaladı. Tipik olarak, anlaşma, hükümetin daha fazla ödeme yapmadan belirli sayıda ürün dozunun mülkiyetini almasını içeriyordu. Örneğin, Amerika Birleşik Devletleri'ndeki Warp Speed Operasyonu'nun himayesinde hükümet, Regeneron'daki COVID-19 aşıları ve terapötikleri ile ilgili araştırmaları sübvanse etti.[147]Johnson ve Johnson, Moderna, AstraZeneca, Novavax, Pfizer ve GSK. Tipik terimler, 400 milyon ila 2 milyar dolarlık araştırma sübvansiyonlarını içeriyordu ve başarıyla geliştirilen herhangi bir COVID-19 aşısının ilk 100 milyon dozunun devlet mülkiyetini içeriyordu.[148]
Amerikan ilaç şirketi Gilead, 23 Mart 2020 tarihinde ABD Gıda ve İlaç Dairesi'nden (FDA) remdesivir için yetim ilaç statüsü aramış ve almıştır. Bu hüküm, vergiler ve devlet ücretlerinden feragatlerin yanı sıra üreticiye güçlendirilmiş ve genişletilmiş yasal tekel hakları vererek 200.000'den az Amerikalıyı etkileyen ilaçların geliştirilmesini teşvik etmeyi amaçlamaktadır.[149][150]Remdesivir, COVID-19'u tedavi etmek için bir adaydır; statü verildiği sırada, 200.000'den az Amerikalı COVID-19'a sahipti, ancak COVID-19 pandemisi ABD'ye ulaştığında rakamlar hızla artıyordu ve eşiği geçmek yakında kaçınılmaz kabul edildi.[149][150]Remdesivir, Gilead tarafından 79 milyon doların üzerinde ABD hükümeti fonu ile geliştirildi.[150]Mayıs 2020'de Gilead, federal hükümete ilk 940.000 doz remdesivir'i ücretsiz olarak sağlayacağını duyurdu.[151]Güçlü kamuoyu tepkileriyle karşılaştıktan sonra Gilead, 25 Mart'ta remdesivir için "yetim ilaç" statüsünden vazgeçti.[152]Gilead, 70'ten fazla ülkede 20 yıllık remdesivir patentlerini elinde tutuyor.[145]Mayıs 2020'de şirket ayrıca, gelişmekte olan ülkeler için remdesivir üretme hakları sağlamak için birkaç jenerik şirketi ve daha geniş jenerik erişim sağlamak için İlaç Patent Havuzu ile görüşmelerde olduğunu duyurdu.[153]
Gelişmekte olan dünya
Patentler
Gelişmekte olan dünyada patentler, düşünüldüğü gibi eleştirildi[kim?] mevcut ilaçlara erişimi azaltmak için.[154]Patentleri ve tıbba evrensel erişimin uzlaştırılması, verimli bir uluslararası fiyat ayrımcılığı politikası gerektirecektir. Ayrıca, Dünya Ticaret Örgütü'nün TRIPS anlaşması kapsamında ülkeler farmasötik ürünlerin patentlenmesine izin vermek zorundadır. 2001 yılında DTÖ, TRIPS anlaşmasının halk sağlığı hedefleri göz önünde bulundurularak okunması gerektiğini gösteren Doha Deklarasyonu'nu kabul etti ve ilaç tekellerini atlatmak için bazı yöntemlere izin veriyor: patentin sona ermesinden önce bile zorunlu lisanslama veya paralel ithalat yoluyla.[155]
Mart 2001'de, 40 çok uluslu ilaç şirketi, bu ilaçların patentli olmasına rağmen, HIV tedavisi için antiretroviral ilaçların (ARV'ler) jenerik üretimine izin veren İlaç Yasası için Güney Afrika'ya karşı dava açtı.[156]HIV, Güney Afrika'da bir salgındı ve o zamanlar ARV'ler hasta başına yıllık 10.000 ABD Doları ile 15.000 ABD Doları arasında mal oluyor. Bu, çoğu Güney Afrika vatandaşı için uygun değildi ve bu nedenle Güney Afrika hükümeti, insanların karşılayabileceğine daha yakın fiyatlarla ARV sağlamayı taahhüt etti. Bunu yapmak için, uyuşturucu patentlerini görmezden gelmeleri ve ülke içinde (zorunlu bir lisans kullanarak) jenerik üretmeleri veya yurt dışından ithal etmeleri gerekir. Halk sağlığı hakları lehine uluslararası protestonun ardından (Sınır Tanımayan Doktorlar tarafından 250.000 imzanın toplanması dahil), birkaç gelişmiş ülkenin (Hollanda, Almanya, Fransa ve daha sonra ABD dahil) hükümetleri Güney Afrika hükümetini destekledi ve dava o yılın Nisan ayında düştü.[157]
2016 yılında GlaxoSmithKline (dünyanın en büyük altıncı ilaç şirketi), bağımsız şirketlerin bu bölgelerde ilaçlarının versiyonlarını yapmasına ve satmasına izin vermek için fakir ülkelerdeki patentlerini düşüreceğini ve böylece halkın bunlara erişimini genişleteceğini duyurdu.[158]GlaxoSmithKline, dünya çapında bir milyar insanı etkileyen artık patent sahibi olmayacakları 50 ülkenin bir listesini yayınladı.
Yardım programları
2011'de en iyi 20 kurumsal hayır bağışından dördü ve en iyi 30 kurumsal hayır bağışından sekizi ilaç üreticilerinden geldi. Kurumsal hayır bağışlarının büyük kısmı (2012 itibariyle %69), çoğunluğu yine ilaç şirketlerinin katkıda bulunduğu bağışlar olan nakit dışı hayırsever bağışlar yoluyla geliyor.[159]
İlaç şirketlerinin yardım programları ve ilaç keşfi ve geliştirme çabaları şunları içerir:
- Afrika'da milyarlarca nehir körlüğü ilacının bağışlandığı "Merck'in Hediyesi"[160]
- Pfizer'ın Güney Afrika'da AIDS için ücretsiz/indirimli flukonazol ve diğer ilaçları hediyesi[161]
- GSK'nın dünya çapında lenfatik filaryazın ortadan kaldırılması için ve buna kadar DSÖ'ye ücretsiz albendazol tabletleri verme taahhüdü.
- 2006 yılında Novartis, dünya çapında kurumsal vatandaşlık girişimlerinde 755 milyon ABD doları taahhüt etti ve özellikle cüzzam, tüberküloz ve sıtmadan etkilenen hastalara ilaç bağışları da dahil olmak üzere İlaca Erişim projeleri aracılığıyla gelişmekte olan dünyada ilaçlara erişimi iyileştirmeye odaklandı; Glivec hasta yardım programları; ve acil tıbbi ihtiyaçları olan büyük insani yardım kuruluşlarını desteklemek için yardım.[162]
Ayrıca bakınız
- Endüstriyel komplekslerin listesi - Ekonomik kavram
- Büyük İlaç komplo teorisi - İlaç endüstrisi hakkında komplo teorileri
- Klinik araştırma - Tıpta klinik araştırma aşaması
- İlaç geliştirme - Pazara yeni bir farmasötik ilaç getirme süreci
- İlaç keşfi - Farmasötik prosedür
- Yasal ilaç ticareti - farmasötik ilaçların üretimi ve satışı
- İlaç şirketlerinin listesi
- Lisanslı üretim - Başka bir yerde geliştirilen teknoloji lisansı altında üretim
- Dış Kaynak Kullanımı - Daha önce dahili görevleri harici bir kuruluşa sözleşme yapmak
- İlaç pazarlaması - İlaç şirketlerinin reklamları
- Eczacılık - Klinik sağlık bilimi
- Eczane yardım yönetimi - Amerika Birleşik Devletleri'nde reçeteli ilaç programlarının yönetimi
- Unitaid - Küresel sağlık girişimi
- Değerleme (finans) § Maddi olmayan duran varlıkların değerlemesi
Referanslar
- McGuire, John L. ; Hasskarl, Horst; Bode, Gerd; Klingmann, Ingrid; Zahn, Manuel (2007). "İlaçlar, Genel Anket". Ullmann'ın Endüstriyel Kimya Ansiklopedisi. Wiley. doi:10.1002/14356007.a19_273.pub2. ISBN 978-3527306732.
- Bozenhardt, Erich H. ; Bozenhardt, Herman F. (18 Ekim 2018). "Dolgudan Çok Mu Şey Istiyorsun?". Pharmaceutical Online (Misafir sütunu). VertMarkets. 17 Kasım 2020'de orijinalinden arşivlendi. Erişim tarihi: 30 Ekim 2018.
İlaç endüstrisinin temel misyonu, diğer tedavilerin yanı sıra, genellikle enjekte edilebilir bir sıvı veya oral katı üreterek hastaların onları tedavi etmesi, aşılaması veya bir semptomu hafifletmesi için ürünler üretmektir.
- Piyasalar, Araştırma ve (31 Mart 2021). "Küresel İlaç Piyasası Raporu 2021: Pazarın 2020'de 1228,45 Milyar Dolardan 2021'de 1250.24 Milyar Dolara Büyümesi Bekleniyor - 2025 ve 2030'a Kadar Uzun Vadeli Tahmin". GlobeNewswire Haber Odası (Basın bülteni). 29 Kasım 2021'de orijinalinden arşivlendi. Erişim tarihi: 29 Kasım 2021.
- Merck, Hoffman-La Roche, Burroughs-Wellcome (şimdi Glaxo Smith Kline'ın bir parçası), Abbott Laboratories, Eli Lilly ve Upjohn (şimdi Pfizer'ın bir parçası) dahil olmak üzere çok uluslu şirketler 1800'lerin ortalarında yerel eczacı olarak başladı.
- "Eczasötik Bilim ve Endüstrinin Ortaya Çıkışı: 1870-1930". Chem Eng Haberleri. 83 (25). 20 Haziran 2005. 10 Kasım 2018 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 23 Temmuz 2022.
- Sneader, Walter (31 Ekim 2005). "13 Nörohormon". İlaç Keşfi: Bir Tarih. John Wiley ve Oğulları. s. 155–156. ISBN 978-0-470-01552-0. Erişim tarihi: 23 Temmuz 2022.
- Rasmussen, Nicolas (2006). "İlk Anti-Depresan Yapmak: Amerikan Tıbbında Amfetamin, 1929-1950". J Hist Med Müttefik Bilim. 61 (3): 288–323. doi:10.1093/jhmas/jrj039. PMID 16492800. S2CID 24974454.
- Rasmussen N (Haziran 2008). "Amerika'nın İlk Amfetamin Salgını 1929–1971". Ben J Halk Sağlığı. 98 (6): 974–985.doi:10.2105/AJPH.2007.110593. PMC 2377281. PMID 18445805.
- Yasiry Z, Shorvon SD (Aralık 2012). "Fenobarbital epilepsi tedavisinde nasıl devrim yarattı: son 100 yılda epilepside fenobarbital tedavinin hikayesi". Epilepsi. 53 (Ek 8): 26–39.doi:10.1111/epi.12026. PMID 23205960. S2CID 8934654.
- López-Muñoz F, Ucha-Udabe R, Alamo C (Aralık 2005). "Klinik tanıtımlarından bir asır sonra barbitüratların tarihi". Nöropsikiyatrik Tedavi.1 (4): 329–43. PMC 2424120. PMID 18568113.
- "1965 Uyuşturucu Bağımlılığı Kontrol Değişiklikleri". NEJM (Yayın). 273 (22): 1222–1223. 25 Kasım 1965. doi:10.1056/NEJM196511252732213.
Sorunun ciddiyetinin farkında olan Gıda ve İlaç İdaresi memurları, bu ülkede yıllık olarak üretilen 9.000.000.000 barbitürat ve amfetamin kapsül ve tabletin yaklaşık yarısının yasadışı kullanıma yönlendirildiğini tahmin ediyor. Bu uyuşturucuların yasadışı satışından elde edilecek karların organize suça bir çekicilik olduğu kanıtlandı, çünkü amfetamin toptan olarak 1000 kapsül başına 1 dolardan daha az bir fiyata satın alınabilir, ancak yasadışı pazarda satıldığında, 1000 başına 30 ila 50 dolar getirir ve bireysel alıcıya perakende olarak satıldığında, bir tablet 10 ila 25 sent kadar getirebilir.
- "Yatıştırıcı-Hipnotik İlaçlar — Barbitüratlar — I". NEJM. 255 (24): 1150–1151. 1956. doi:10.1056/NEJM195612132552409. PMID 13378632.
E tarafından ilaca sokulan barbitüratlar. 1903'te Fischer ve J. von Mering, kesinlikle tıpta en yaygın kullanılan ve kötüye kullanılan ilaçlar arasındadır. Her yıl yaklaşık 400 ton bu ajanlardan üretilir; bu, her birine 0.1-gm'lik bir doz verilirse, o dönem boyunca her gece yaklaşık 9.000.000 kişiyi uyutmak için yeterlidir.
- Rosenfeld L (Aralık 2002). "İnsülin: keşif ve tartışma". Clin Kimya. 48 (12): 2270–88. doi:10.1093/clinchem/48.12.2270. PMID 12446492.
- "Önde Gelen Ölüm Nedenleri, 1900-1998" (PDF). CDC.gov. 13 Aralık 2020'de orijinalinden arşivlendi (PDF). Erişim tarihi: 23 Temmuz 2022.
- Anderson, Robert N. (13 Aralık 1999). "Amerika Birleşik Devletleri Yaşam Tabloları, 1997" (PDF). Ulusal Hayati İstatistik Raporları. 47 (28): 1–37.PMID 10635683. 25 Ekim 2020'de orijinalinden (PDF) arşivlendi. Erişim tarihi: 23 Temmuz 2022.
- Sepkowitz, Kent A. (Temmuz 2011). "Salvarsan'ın yüz yılı". N. İngilizce J. Med. (Perspektif). 365 (4): 291–3. doi:10.1056/NEJMp1105345. PMID 21793743.
- Williams, KJ (1 Ağustos 2009). "İlk sihirli mermi olan arsfenamin kullanarak 'kemoterapi'nin tanıtımı". J. R. Soc. Med. 102 (8): 343–348.doi:10.1258/jrsm.2009.09k036. ISSN 0141-0768. PMC 2726818.PMID 19679737.
- Aminov, Rüstam I. (8 Aralık 2010). "Antibiyotik çağının kısa bir tarihi: öğrenilen dersler ve gelecek için zorluklar". Ön. Mikrobiol. 1: 134.doi:10.3389/fmicb.2010.00134. PMC 3109405. PMID 21687759.
- Hager, Thomas (2006). Mikroskop Altındaki Şeytan (1. baskı). New York: Harmony Kitapları. ISBN 978-1-4000-8213-1.
- "Fizyoloji veya Tıpta Tüm Nobel Ödülleri". Nobel Ödülü. Erişim tarihi: 22 Temmuz 2022.
- Cutler, David M. ; Meara, Ellen (Ekim 2001). 20. Yüzyılda Ölümlerin Yaş Dağılımındaki Değişiklikler (PDF) (Rapor). Ulusal Ekonomik Araştırma Bürosu. doi:10.3386/w8556. Erişim tarihi: 23 Temmuz 2022.
- Klein, Herbert (2012). Amerika Birleşik Devletleri'nin Nüfus Tarihi. Cambridge Üniversitesi Yayınları. s. 167.
- Parascandola, John (1980). Antibiyotiklerin tarihi: bir sempozyum. Amerikan Eczacılık Tarihi Enstitüsü No. 5. ISBN 978-0-931292-08-8.
- "Difteri — Zaman Çizelgeleri — Aşıların Tarihi". 14 Mayıs 2016 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 24 Şubat 2022.
- Ii, Thomas H. Maugh (13 Nisan 2005). "Maurice R. Hilleman, 85; Bilim İnsanı Milyonlarca Hayat Kurtaran Birçok Aşı Geliştirdi - Los Angeles Times". Los Angeles Times. 7 Kasım 2014 tarihinde orijinalindenarşivlenmiştir.
- "ABD'de Önemli Tarihler Gıda ve İlaç Hukuku Tarihi". Gıda ve İlaç İdaresi. 6 Mart 2013 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 16 Aralık 2019.
- "FDAReview.org, Bağımsız Enstitü'nün bir projesi". 2 Aralık 2015 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 24 Şubat 2022.
- "Sülfanilamid Felaketi". Gıda ve İlaç İdaresi. 25 Kasım 2020'de orijinalinden arşivlendi. Erişim tarihi: 16 Aralık 2019.
- "FDA Tarihi - Bölüm II". Gıda ve İlaç İdaresi. 1 Ocak 2018 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 16 Aralık 2019.
- Zaffiri L, Gardner J, Toledo-Pereyra LH (Nisan 2012). "Antibiyotiklerin tarihi. Salvarsan'dan sefalosporinlere". J Yatırım Surg. 25 (2): 67–77.doi:10.3109/08941939.2012.664099. PMID 22439833. S2CID 30538825.
- Hamilton-Miller JM (Mart 2008). "Yarı sentetik penisilinlerin ve sefalosporinlerin gelişimi". Int. J. Antimikrob. Ajanlar. 31 (3): 189–92.doi:10.1016/j.ijantimicag.2007.11.010. PMİD 18248798.
- Abraham EP (1987). "Sefalosporinler 1945-1986". İlaçlar. 34 Suppl 2 (Ek 2): 1–14. doi:10.2165/00003495-198700342-00003. PMID 3319494.S2CID 12014890.
- Kingston W (Temmuz 2004). "Streptomisin, Schatz v. Waksman ve keşif için kredi dengesi". J Hist Med Müttefik Bilim. 59 (3): 441–62.doi:10.1093/jhmas/jrh091. PMID 15270337. S2CID 27465970.
- Nelson ML, Levy SB (Aralık 2011). "Tetrasiklinlerin tarihi". Ann. N. Y. Acad. Bilim. 1241 (1): 17–32.Bibcode:2011NYASA1241...17N.doi:10.1111/j.1749-6632.2011.06354.x.PMID 22191524. S2CID 34647314.
- "ERITROMISIN". Br Med J. 2 (4793): 1085–6. Kasım 1952.doi:10.1136/bmj.2.4793.1085. PMC 2022076. PMID 12987755.
- Anderson, Rosaleen (2012). Antibakteriyel ajanlar kimyası, etki şekli, direnç mekanizmaları ve klinik uygulamalar. Oxford: WiBlackwell. ISBN 9780470972458.
- Federal Ticaret Komisyonu Antibiyotik Üretimi Raporu, Haziran 1958 (Washington D.C., Devlet Baskı Ofisi, 1958) sayfalar 98-120
- Federal Ticaret Komisyonu Antibiyotik Üretimi Raporu, Haziran 1958 (Washington D.C., Hükümet Matbaası, 1958) sayfa 277
- Anderson, Robert N. (13 Aralık 1999). "Amerika Birleşik Devletleri Yaşam Tabloları, 1997" (PDF). Ulusal Hayati İstatistik Raporları: Hastalık Kontrol ve Önleme Merkezlerinden, Ulusal Sağlık İstatistikleri Merkezi'nden, Ulusal Hayati İstatistik Sisteminden. 47 (28): 1–37. PMID 10635683. 25 Ekim 2020'de orijinalinden arşivlendi (PDF). Erişim tarihi: 8 Eylül 2017.
- Cutler, David; Meara, Ellen (Ekim 2001). "20. Yüzyılda Ölümlerin Yaş Dağılımındaki Değişiklikler" (PDF). NBER Çalışma Kağıdı No. 8556. doi:10.3386/w8556. 30 Temmuz 2020'de orijinalinden arşivlendi (PDF).Erişim tarihi: 24 Şubat 2022.
- SWEET BH, HILLEMAN MR (Kasım 1960). "Vakuolasyon virüsü, S.V. 40".Proc. Soc. Uzman Biyol. Med. 105 (2): 420–7. doi:10.3181/00379727-105-26128. PMID 13774265. S2CID 38744505.
- Shah K, Nathanson N (Ocak 1976). "İnsanın SV40'a maruz kalması: inceleme ve yorum". Am. J. Epidemiol. 103 (1): 1–12.doi:10.1093/oxfordjournals.aje.a112197. PMID 174424.
- "Çalışmalar: SV40'ın Kanserle İlişkili Olduğuna Dair Kanıt Yok - Ulusal Kanser Enstitüsü". 28 Ekim 2014 tarihinde orijinalinden arşivlenmiştir.
- "Aşıların Tarihi — Philadelphia Hekimler Koleji'nin Bir Aşı Tarihi Projesi".19 Şubat 2022'de orijinalinden arşivlendi. Erişim tarihi: 24 Şubat 2022.
- "Kızamık, Kızamıkçık, Konjenital Kızamıkçık Sendromu ve Kabakulakların Önlenmesi, 2013". 10 Kasım 2014 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 8 Eylül 2017.
- Bloch AB, Orenstein WA, Stetler HC, et al. (1985). "Amerika Birleşik Devletleri'nde kızamık aşısının sağlığa etkisi". Pediatri. 76 (4): 524–32.doi:10.1542/peds.76.4.524. PMID 3931045. S2CID 6512947.
- Insull W (Ocak 2009). "Ateroskleroz patolojisi: plak gelişimi ve tıbbi tedaviye plak tepkileri". Amerikan Tıp Dergisi. 122 (1 Suppl): S3–S14.doi:10.1016/j.amjmed.2008.10.013. PMID 19110086.
- Gaddam KK, Verma A, Thompson M, Amin R, Ventura H (Mayıs 2009)."Çeşitli formlarında hipertansiyon ve kalp yetmezliği". Kuzey Amerika Tıp Klinikleri. 93 (3): 665–80. doi:10.1016/j.mcna.2009.02.05. PMID 19427498. Erişim tarihi: 20 Haziran 2009.
- Agabiti-Rosei E (Eylül 2008). "Makro- mikro sirkülasyondan: hipertansiyon ve diyabetteki faydalar". Hipertansiyon Dergisi. 26 (Ek 3): S15–21. doi:10.1097/01.hjh.0000334602.71005.52. PMID 19363848.
- Murphy BP, Stanton T, Dunn FG (Mayıs 2009). "Hipertansiyon ve miyokardiyal iskemi". Kuzey Amerika Tıp Klinikleri. 93 (3): 681–95. doi:10.1016/j.mcna.2009.02.003. PMID 19427499. Erişim tarihi: 20 Haziran 2009.
- Beyaz WB (Mayıs 2009). "Hastanın hipertansiyon ve artrit ağrısı tedavisi probleminin tanımlanması". Amerikan Tıp Dergisi. 122 (5 Suppl): S3–9. doi:10.1016/j.amjmed.2009.03.002. PMID 19393824.
- Truong LD, Shen SS, Park MH, Krishnan B (Şubat 2009). "Nefrektomi örneklerinde neoplastik olmayan lezyonların teşhisi". Patoloji ve Laboratuvar Tıbbı Arşivleri. 133 (2): 189–200. doi:10.5858/133.2.189.PMID 19195963. Erişim tarihi: 20 Haziran 2009.
- Tracy RE, White S (Şubat 2002). "Otopside adrenokortikal nodüler hiperplaziyi ölçmek için bir yöntem: yöntemin hipertansiyon ve aterosklerozu aydınlatmada bazı kullanımları". Tanısal Patoloji Yıllıkları. 6 (1): 20–9. doi:10.1053/adpa.2002.30606. PMID 11842376.
- Aronow WS (Ağustos 2008). "Hipertansiyon ve yaşlı diyabetik". Geriatrik Tıpta Klinikler. 24 (3): 489–501, vi–vii.doi:10.1016/j.cger.2008.03.001.PMID 18672184. Erişim tarihi: 20 Haziran 2009.
- Gardner AW, Afaq A (2008). "Alt Ekstremite Periferik Arter Hastalığının Yönetimi". Kardiyopulmoner Rehabilitasyon ve Önleme Dergisi. 28 (6): 349–57. doi:10.1097/HCR.0b013e31818c3b96. PMC 2743684. PMID 19008688.
- Novo S, Lunetta M, Evola S, Novo G (Ocak 2009). "ARB'lerin kan hipertansiyon tedavisindeki ve kardiyovasküler olayların önlenmesindeki rolü". Mevcut Ilaç Hedefleri. 10 (1): 20–5. doi:10.2174/138945009787122897. PMID 19149532. 12 Ocak 2013 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 20 Haziran 2009.
- Craig WM (1939). "Hipertansiyonun cerrahi tedavisi". Br Med J. 2 (4120): 1215–9. doi:10.1136/bmj.2.4120.1215. PMC 2178707. PMID 20782854.
- Sneader, Walter (2005). İlaç Keşfi. Bir Tarih. New York: Wiley. s. 371.
- Beyer KH (1993). "Klorotiyazid. Tiyazidler antihipertansif tedavi olarak nasıl gelişti". Hipertansiyon. 22 (3): 388–91.doi:10.1161/01.hyp.22.3.388. PMID 8349332.
- BORHANI NO, HECHTER HH (1964). "Kaliforniya'da CVR Hastalığı Ölümlerinde Son Değişiklikler: Epidemiyolojik Bir Değerlendirme". Halk Sağlığı Temsilcisi 79 (2): 147–60. doi:10.2307/4592077. JSTOR 4592077. PMC 1915335. PMID 14119789.
- "Lasker Vakfı - Ödüller". 23 Aralık 2015 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 24 Şubat 2022.
- Wright, James M. ; Musini, Vijaya M. ; Gill, Rupam (18 Nisan 2018)."Hipertansiyon için birinci basamak ilaçlar". Cochrane Sistematik İncelemeler Veri Tabanı. 2018 (4): CD001841. doi:10.1002/14651858. CD001841.pub3. ISSN 1469-493X. PMC 6513559. PMID 29667175.
- Stason WB, Cannon PJ, Heinemann HO, Laragh JH (Kasım 1966)."Furosemid. Diüretik etkisinin klinik bir değerlendirmesi". Dolaşım. 34 (5): 910–20. doi:10.1161/01.cir.34.5.910. PMİD 5332332. S2CID 886870.
- Black JW, Crowther AF, Shanks RG, Smith LH, Dornhorst AC (1964). "Yeni bir adrenerjik betareseptör antagonisti". Lancet. 283 (7342): 1080–1081. doi:10.1016/S0140-6736(64)91275-9. PMID 14132613.
- Lv J, Perkovic V, Foote CV, Craig ME, Craig JC, Strippoli GF (2012). "Diyabetik böbrek hastalığını önlemek için antihipertansif ajanlar". Cochrane Veritabanı Sistemi Rev. 12: CD004136.doi:10.1002/14651858. CD004136.pub3. PMID 23235603.
- "Doğum kontrol hapının kısa bir tarihi - Hap zaman çizelgesi | Bilinmesi Gerekenler | PBS". PBS. 7 Mayıs 2010. 19 Ocak 2018 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 8 Eylül 2017.
- Dergi, Smithsonian. "Oral Kontraseptif Neden Sadece "Hap" Olarak Bilinir". Smithsonian Dergisi. smithsonianmag.com. 28 Nisan 2021'de orijinalinden arşivlendi. Erişim tarihi: 24 Şubat 2022.
- "BBC Haberleri | SAĞLIK | Hapın kısa tarihi". 6 Temmuz 2021'de orijinalinden arşivlendi. Erişim tarihi: 24 Şubat 2022.
- "FDA'nın İlk Oral Kontraseptif Onayı, Enovid". Gıda ve İlaç İdaresi. 23 Temmuz 2017 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 16 Aralık 2019.
- Cafe, Rebecca (4 Aralık 2011). "BBC News - Kontraseptif hap İngiltere'yi nasıl değiştirdi". BBC Haberleri. 16 Haziran 2019'da orijinalinden arşivlendi. Erişim tarihi: 21 Haziran 2018.
- "Broşür: Amerika Birleşik Devletleri'nde Uyuşturucu Düzenlemesinin Tarihi". Gıda ve İlaç İdaresi. 23 Temmuz 2017 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 16 Aralık 2019.
- Tobert, Jonathan A. (TEMMUZ 2003). "Lovastatin ve ötesi: HMG-CoA redüktaz inhibitörlerinin öyküsü". Nature Reviews İlaç Keşfi. 2 (7): 517–526. doi:10.1038/nrd1112. ISSN 1474-1776. PMID 12815379. S2CID 3344720.
- Endo A (1 Kasım 1992). "HMG-CoA redüktaz inhibitörlerinin keşfi ve geliştirilmesi". Lipid Araştırmaları Dergisi. 33 (11): 1569–82.doi:10.1016/S0022-2275(20)41379-3. PMID 1464741.
- Endo, Akira (2004). "Statinlerin kökeni". Uluslararası Kongre Serisi. 1262: 3–8. doi:10.1016/j.ics.2003.12.099.
- Scandinaviansimvastatinsurvival (Kasım 1994). "Koroner kalp hastalığı olan 4444 hastada rastgele kolesterol düşürme çalışması: İskandinav Simvastatin Sağkalım Çalışması (4S)". Lancet. 344 (8934): 1383–9.doi:10.1016/S0140-6736(94)90566-5. PMID 7968073. S2CID 5965882.
- "National Inventors Hall of Fame Honors 2012 Inductees". PRNewswire. 12 Mayıs 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Mayıs 2014.
- "Bir Bilim İnsanı Küflerin İlgisini Nasıl Buldu? Wall Street Dergisi. 24 Şubat 2022'de orijinalinden arşivlendi. Erişim tarihi: 11 Mayıs 2014.
- "En İyi Küresel İlaç Şirketi Raporu - İlaç 1000"(PDF). Torreya. Erişim tarihi: 19 Ağustos 2022.
- "En İyi Küresel İlaç Şirketi Raporu" (PDF). İlaç 1000. Kasım 2021. Erişim tarihi: 29 Aralık 2022.
- Alvarado, Delilah; Pagliarulo, Ned (8 Ocak 2024). "Yıllı biyoteknoloji işten çıkarmaları endüstriyi kıvılcım arıyor". BioPharma Dalışı. Erişim tarihi: 10 Ocak 2024.
- Bell, Jacob (20 Aralık 2022). "Biotech M&A geri dönüyor. İşte en son anlaşma". BiopharmaDive. 24 Aralık 2022'de orijinalinden arşivlendi. Erişim tarihi: 23 Aralık 2022.
- "Yıllık Etki Raporu". Tufts İlaç Geliştirme Çalışmaları Merkezi. 3 Şubat 2022'de orijinalinden arşivlendi. Erişim tarihi: 24 Şubat 2022.
- "İlaç Endüstrisi Rakamlarla Anahtar Veriler 2021" (PDF). Avrupa İlaç Endüstrileri ve Dernekleri Federasyonu. 30 Nisan 2022'de alındı.
- Dış Kaynak-Pharma.com (25 Mayıs 2011). "Pfizer, CRO sektörünün en son stratejik anlaşmalarında Parexel ve Icon ile birlikte çalışıyor".Outsourcing-Pharma.com. 11 Ekim 2013 tarihinde orijinalinden arşivlendi. Erişim tarihi: 24 Şubat 2022.
- "FDA Geçen Yıl Kaç Yeni İlaç Onayladı?". pharmalot.com. 8 Mayıs 2011 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 23 Nisan 2011.
- "Araştırma". 20 Temmuz 2011 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 24 Kasım 2006.
- Perry, Susan (8 Ağustos 2012). "BMJ 2012'de Donald Light ve Joel Lexchin;345:e4348, alıntı: BMJ yazarları, Big Pharma'nın 'inovasyon krizi' iddiasının bir efsane olduğunu söylüyor". MinnPost. 11 Ağustos 2012 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 8 Ağustos 2012.
- "PhRMA Hakkında - PhRMA". 4 Ocak 2013 tarihinde orijinalindenarşivlenmiştir. Erişim tarihi: 23 Nisan 2011.
- "Has the Pharmaceutical Blockbuster Model Gone Bust?". bain.com.24 Mart 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 19 Mayıs 2016.
- Harper, Matthew (10 Şubat 2012). "Yeni Ilaçlar Icat Etmenin Gerçekten Şaşırtıcı Maliyeti". Forbes. 9 Aralık 2020'de orijinalinden arşivlendi. Erişim tarihi: 8 Eylül 2017.
- IMS Sağlık (18 Haziran 2015). "Avrupalı biyoteknoloji şirketleri yeterince korunuyor mu?". Rekabetçi Zeka Portalı. 30 Haziran 2015 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 27 Haziran 2015.
- Liberti L, McAuslane JN, Walker S (2011). "Yeni İlaçların Fayda-Risk Değerlendirmesinin Standartlaştırılması: İlaç Sağlık Profesyonelleri için Çerçevelerin Pratik Uygulamaları". Pharm Med. 25 (3): 139–46.doi:10.1007/BF03256855. S2CID 45729390. 6 Şubat 2012 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 18 Ekim 2011.
- "Elektronik Turuncu Kitap". ABD Gıda ve İlaç İdaresi. 7 Nisan 2020'de orijinalinden arşivlendi. Erişim tarihi: 31 Mayıs 2007.
- "Yetim Uyuşturucu Yasası (değiştirildiği gibi)". ABD Gıda ve İlaç İdaresi.7 Nisan 2020'de orijinalinden arşivlendi. Erişim tarihi: 24 Eylül 2007.
- "2022 gelirine göre en iyi 20 ilaç şirketi".
- "Standardseite der Domain www.vfa.de" (PDF). 11 Ağustos 2016 tarihinde orijinalinden (PDF) arşivlendi. Erişim tarihi: 24 Mart 2008.
- Herper, Matthew & Kang, Peter (22 Mart 2006). "Dünyanın En Çok Satan On İlacı". Forbes. 5 Mayıs 2006 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 31 Mayıs 2007.
- "Daha İyi Sağlık Hizmetleri Performansı için Bağlantılı Çözümler Yaratmak". IMS Sağlığı. 10 Mayıs 2020'de orijinalinden (PDF) arşivlendi. Erişim tarihi: 23 Şubat 2022.
- Kollewe, Julia (27 Mart 2014). "Dünyanın en çok satan 10 reçeteli ilacı geçen yıl 75 milyar dolar kazandı". Guardian. 7 Nisan 2020'de orijinalinden arşivlendi. Erişim tarihi: 12 Aralık 2016.
- "Satışlara Göre 2013 için En İyi 100 İlaç - ABD İlaç İstatistikleri". 31 Mart 2014 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 23 Ocak 2018.
- "IMS Sağlık Tahminleri 2007'de Küresel İlaç Pazarı için Yüzde 5 ila 6 Büyüme". IMS Sağlığı. 24 Ekim 2006. 3 Mayıs 2011 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 19 Haziran 2007.
- Sıkça Sorulan Sorular (SSS) 25 Şubat 2013 tarihinde Wayback Machine sitesinde arşivlendi.
- "2006'da Yeni İlaç Onayları" (PDF). Mart 2007. 28 Şubat 2008 tarihinde orijinalinden (PDF) arşivlenmiştir. Erişim tarihi: 23 Şubat 2008.
- "ABD'de Yetkili Jeneriklerin Değerlendirilmesi" (PDF). IMS Danışmanlık. Haziran 2006. 28 Şubat 2008 tarihinde orijinalinden (PDF) arşivlenmiştir. Erişim tarihi: 23 Şubat 2008.
- "Sanofi ABD'de 1.700'ü işten çıkardı". İlaç Keşfi ve Geliştirme. 11 Eylül 2011 tarihinde orijinalinden arşivlendi. Erişim tarihi: 24 Şubat 2022.
- "2007 Sağlık ve Beslenme - Nüfus Sayımı" (PDF). ABD Sayım Bürosu. 31 Temmuz 2020'de orijinalinden arşivlendi (PDF). Erişim tarihi: 19 Mayıs 2016.
- Goldacre, Ben (2014). Kötü ilaç: ilaç şirketleri doktorları nasıl yanlış yönlendiriyor ve hastalara nasıl zarar veriyor (First American Paperback ed.). Macmillan.ISBN 9780865478060.
- Kaufman, Marc (6 Mayıs 2005). "Merck CEO'su İlaç Sondası Devam Ederken İstifa Etti". Washington Post. 9 Kasım 2020'de orijinalinden arşivlendi. Erişim tarihi: 23 Mayıs 2007.
- "İlaç Lobisi Yok İkincisi: İlaç endüstrisi Washington'da nasıl yoluna giriyor". publicintegrity.org. 7 Temmuz 2005. 9 Haziran 2007 tarihinde orijinalindenarşivlenmiştir. Erişim tarihi: 23 Mayıs 2007.
- Moynihan, R. (29 Mayıs 2003). "İlaç şirketi eğitim sponsorluğu, maliyetinin bir kısmıyla değiştirilebilir". BMJ. 326 (7400): 1163.doi:10.1136/bmj.326.7400.1163. PMC 1126044. PMID 12775595.
- "Dr. Ücretsiz Öğle Yemeği Yok". Jones Ana. 16 Kasım 2020'de orijinalinden arşivlendi. Erişim tarihi: 19 Mayıs 2016.
- Moynihan, Ray; Cassels, Alan (2005). Hastalık Satmak: İlaç Şirketleri Hepimizi Nasıl Hastaya Dönüştürüyor? Karga Yuvası, N.S.W.: Allen & Unwin. ISBN 978-1-74114-579-3.
- "Hastalık Tağdırma Üzerine Makaleler Koleksiyonu". Halk Bilim Kütüphanesi. 7 Haziran 2007 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 23 Mayıs 2007.
- "İlaç Pazar Araştırması, Eğilimler Ve Analiz Raporları". literated.com. 19 Ocak 2016 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 17 Ocak 2016.
- Buchkowsky, SS; Jewesson, PJ (Nisan 2004). "20 yılı aşkın süredir endüstri sponsorluğu ve klinik araştırmaların yazarlığı". Ann Pharmacother.38 (4): 579–85. doi:10.1345/aph.1D267. PMID 14982982. S2CID 43544256.
- Perlis RH, Perlis CS, Wu Y, Hwang C, Joseph M, Nierenberg AA (Ekim 2005). "Psikiyatride klinik çalışmaların raporlanmasında endüstri sponsorluğu ve mali çıkar çatışması". Ben J Psikiyatri. 162 (10): 1957–60.doi:10.1176/appi.ajp.162.10.1957. PMID 16199844.
- Tungaraza, T; Poole, R (Temmuz 2007). "İlaç şirketi yazarlığının ve sponsorluğunun ilaç deneme sonuçları üzerindeki etkisi". Br J Psikiyatri.191 (1): 82–3.doi:10.1192/bjp.bp.106.024547. PMID 17602130.
- Healy, D (2006). "En Son Mani: Bipolar Bozukluk Satmak". PLOS Med. 3 (4): e185. doi:10.1371/journal.pmed.0030185. PMC 1434505. PMID 16597178.
- Cosgrove, Lisa; Krimsky, Sheldon; Vijayaraghavan, Manisha; Schneider, Lisa (2006). "DSM-IV Panel Üyeleri ve İlaç Endüstrisi arasındaki Finansal Bağlar". Psikoterapi ve Psikosomatik. 75 (3): 154–160. doi:10.1159/000091772. PMID 16636630. S2CID 11909535.
- "Açık Ödemeler". Şubat 2019. 22 Şubat 2022'de orijinalinden arşivlendi. Erişim tarihi: 24 Şubat 2022.
- Lipton, Eric; Thomas, Katie (29 Mayıs 2017). "Uyuşturucu Lobicilerinin Fiyatlar İçin Savaş Çığlığı: Diğerlerini Suçlayın". New York Times. 20 Kasım 2020'de orijinalinden arşivlendi. Erişim tarihi: 30 Mayıs 2017.
- Morgan, Steven G.; Bathula, Hannah S. ; Ay, Suerie (2020). "İlaçların fiyatlandırılması sağlık sistemleri için büyük bir zorluk haline geliyor".BMJ.368: l4627. doi:10.1136/bmj.l4627. PMID 31932289. S2CID 210192662. 27 Kasım 2020'de orijinalinden arşivlendi. Erişim tarihi: 14 Kasım 2020.
- "Yüksek İlaç Fiyatları ve Hasta Maliyetleri: Milyonlarca Hayat ve Milyarlarca Dolar Kayboldu". www.cidsa.org. Bilgilendirilmiş İlaç Harcama Analizi için Batı Sağlık Konseyi. 18 Kasım 2020. Erişim tarihi: 20 Şubat 2023.
- Goldacre, Ben (2014). Kötü ilaç: ilaç şirketleri doktorları nasıl yanlış yönlendiriyor ve hastalara nasıl zarar veriyor (First American Paperback ed.). Macmillan. s. 123–124. ISBN 9780865478060.
- "Arşivlenmiş kopya" (PDF). Bilim ve Teknoloji Politikası Ofisi. 21 Ocak 2017 tarihinde orijinalinden arşivlendi (PDF). 1 Mart 2021'de alındı - Ulusal Arşivler aracılığıyla.
{{cite web}}: CS1 maint: başlık olarak arşivlenmiş kopya (bağlantı) - "2006 Kamu Raporuna Mali Suçlar". FBI. 2006. 29 Mayıs 2016 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 28 Temmuz 2016.
- "FBI-Sağlık Dolandırıcılığı". FBI. 2 Temmuz 2016 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 28 Temmuz 2016.
- "Adalet Bakanlığı". Adalet Bakanlığı. 19 Mart 2015. 9 Kasım 2014 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 22 Kasım 2020.
- Wilson, Duff (2 Ekim 2010). "Yan Etkiler Davaları Içerebilir". New York Times. 23 Haziran 2017 tarihinde orijinalinden arşivlendi. Erişim tarihi: 25 Şubat 2017.
- "GlaxoSmithKline". BBC Haberleri. 4 Temmuz 2012. 17 Kasım 2020'de orijinalinden arşivlendi. Erişim tarihi: 21 Haziran 2018.
- "GlaxoSmithKline ABD'de 3 Milyar Dolar Ödemeyi Kabul Ediyor Uyuşturucu Yerleşimi". Bloomberg. 2 Temmuz 2012. 14 Mayıs 2014 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 11 Mart 2017.
- Mogul, Fred (2 Temmuz 2012). "NY, GlaxoSmithKlein Yerleşiminde Milyonlar Alacak". WNYC. 19 Nisan 2013 tarihinde orijinalindenarşivlenmiştir. Erişim tarihi: 2 Temmuz 2012.
- "BBC News -GlaxoSmithKline, ABD uyuşturucu dolandırıcılık skandalında 3 milyar dolar ödeyecek". BBC Çevrimiçi. 2 Temmuz 2012. 17 Kasım 2020'de orijinalinden arşivlendi. Erişim tarihi: 2 Temmuz 2012.
- Thomas, Katie & Schmidt, Michael S. (2 Temmuz 2012). "Glaxo, Dolandırıcılık Uzlaşmasında 3 Milyar Dolar Ödemeyi Kabul Etti". New York Times. 2 Mart 2017 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 3 Temmuz 2012.
- "İlaç Endüstrisine Karşı Cezai ve Sivil Cezaların Hızla Artırılması: 1991-2010". citizen.org. 16 Mayıs 2016 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 19 Mayıs 2016.
- Thomas, Katie; Schmidt, Michael S. (2 Temmuz 2012). "GlaxoSmithKline Dolandırıcılık Uzlaşmasında 3 Milyar Dolar Ödemeyi Kabul Ediyor". The New York Times. 12 Kasım 2020'de orijinalinden arşivlendi. Erişim tarihi: 25 Şubat 2017.
- "GlaxoSmithKline, Dolandırıcılık İddialarını ve Güvenlik Verilerini Bildirmemeyi Çözmek için Suçlu İddia Edecek ve 3 Milyar Dolar Ödeyecek". 2 Temmuz 2012. 9 Eylül 2014 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 22 Kasım 2020.
- "ADALET BAKANLIĞI EN BÜYÜK SAĞLIK DOLANDIRICILIĞINI AÇIKLADI" (PDF). ABD Adalet Bakanlığı. 2 Aralık 2020'de orijinalinden arşivlendi (PDF). Erişim tarihi: 19 Mayıs 2016.
- "Abbott Labs, Depakote'nin Etiket Dışı Tanıtımına İlişkin Cezai ve Sivil Soruşturmaları Çözmek için 1,5 Milyar Dolar Ödeyecek". 7 Mayıs 2012.21 Ağustos 2014 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 22 Kasım 2020.
- "#09-038: Eli Lilly ve Şirket, Zyprexa'nın Etiket Dışı Tanıtımı İddialarını Çözmek için 1.415 Milyar Dolar Ödemeyi Kabul Etti (2009-01-15)". 13 Mart 2016 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 22 Kasım 2020.
- Drazen, Jeffrey M. (2015). "Ticari-Akademik Arayüzün Tekrar Gözden Geçirilmesi". New England Tıp Dergisi. 372 (19): 1853–1854.doi:10.1056/NEJMe1503623. PMID 25946285.
- Rosenbaum, Lisa (2015). "Noktaları Yeniden Birleştirmek - Endüstri-Hekim İlişkilerini Yeniden Yorumlamak". New England Tıp Dergisi. 372 (19): 1860–1864. doi:10.1056/NEJMms1502493. PMID 25946288.
- "Covid aşısı öncüleri: Ne kadara mal oldular, onları kim satın aldı ve nasıl depolandılar". CNBC. 17 Kasım 2020. 1 Aralık 2020'de orijinalinden arşivlendi. Erişim tarihi: 2 Aralık 2020.
- Henninger, Daniel (2 Aralık 2020). "Görüş | İlaç, Covid Aşıları için Nobel Barış Ödülü'nü Hak Ediyor". Wall Street Journal. 3 Şubat 2021'de orijinalinden arşivlendi. Erişim tarihi: 4 Aralık 2020.
- "MSF, COVID-19 ilaçları ve aşıları konusunda vurgunculuk yok" diyor.Sınır Tanımayan Doktorlar (MSF) Uluslararası. 26 Kasım 2021'de orijinalinden arşivlendi. Erişim tarihi: 22 Nisan 2020.
- Mazzucato, Mariana; Momenghalibaf, Azzi (18 Mart 2020). "Uyuşturucu Şirketleri Koronavirüsten Cinayet Edecek". The New York Times. 23 Kasım 2020'de orijinalinden arşivlendi. Erişim tarihi: 22 Nisan 2020.
- "HHS, DOD, COVID-19 Araştırmacı Terapötik Tedavinin Büyük Ölçekli Üretim Gösteri Projesinde Regeneron ile İşbirliği Yapıyor". 6 Temmuz 2020. 18 Aralık 2020'de orijinalinden arşivlendi. Erişim tarihi: 2 Aralık 2020.
- "COVID-19 Aşıları". 12 Aralık 2020. 19 Aralık 2020'de orijinalinden arşivlendi. Erişim tarihi: 2 Aralık 2020.
- Lupkin, Sidney (24 Mart 2020). "FDA, Nadir Hastalık Tedavileri İçin Deneysel Koronavirüs İlaç Faydaları Sağlıyor". NPR. 14 Aralık 2020'de orijinalinden arşivlendi. Erişim tarihi: 24 Mart 2020.
- Conley, Julia (24 Mart 2020). "'Bu Büyük Bir Skandal': Trump FDA, İlaç Şirketine Umut Veren Koronavirüs İlacına Özel İddiasını Verdi". Ortak Rüyalar. 8 Aralık 2020'de orijinalinden arşivlendi. Erişim tarihi: 22 Nisan 2020.
- Boodman, Eric (18 Mayıs 2020). "Gilead, ABD hastaneleri için Covid-19 ilaç remdesivir bağışını artırıyor". statnews.com. 20 Aralık 2020'de orijinalinden arşivlendi. Erişim tarihi: 19 Temmuz 2020.
- Lawson, Alex (25 Mart 2020). "Büyük İlaçların COVID-19 Tedavilerini Vurgunculuk Yaparak Öldürmesine İzin Vermeyin". Ortak Rüyalar. 9 Kasım 2020'de orijinalinden arşivlendi. Erişim tarihi: 22 Nisan 2020.
- "Gilead Sciences, Araştırmacı Antiviral Remdesivir'in Küresel Tedarikini Genişletmeye İlişkin Beyanı | Gilead". 11 Aralık 2020'de orijinalinden arşivlendi. Erişim tarihi: 16 Temmuz 2020.
- Örneğin bakınız: 't Hoen, Ellen. "TRIPS, İlaç Patentleri ve Temel İlaçlara Erişim: Seattle'dan Doha'ya Uzun Bir Yol". Chicago Uluslararası Hukuk Dergisi, 27(43), 2002; Musungu, Sisule F. ve Cecilia Oh. "Gelişmekte Olan Ülkeler Tarafından TRIPS'te Esnekliklerin Kullanımı: İlaçlara Erişim Sağlayabilirler mi?" Fikri Mülkiyet Hakları, Yenilik ve Halk Sağlığı Komisyonu, Dünya Sağlık Örgütü, 2005.
- "TRIPS anlaşması ve halk sağlığı hakkında deklarasyon". Dünya Ticaret Örgütü. 20 Haziran 2016 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 19 Mayıs 2016.
- İlaç Üreticileri Derneği v. Güney Afrika Başkanı (PMA), 2002 (2) SA 674 (CC) (S. Afrika).
- Helfer, Laurence R. ; Austin, Graeme W. (7 Mart 2011). İnsan Hakları ve Fikri Mülkiyet: Küresel Arayüzün Haritalanması. Cambridge Üniversitesi Yayınları. s. 145–148. ISBN 978-1-139-49691-9. 16 Kasım 2020'de orijinalinden arşivlendi. Erişim tarihi: 28 Temmuz 2016.
- "GlaxoSmithKline 'daha iyi ilaç erişimi için fakir ülkelerdeki patentleri bırakacak'". BBC Haberleri. 9 Kasım 2020'de orijinalinden arşivlendi. Erişim tarihi: 19 Mayıs 2016.
- "Kurumsal Bağışlar için Tampon Yıl Kâr Motiflerini Ortaya Çıkarıyor".corpwatch.org. 11 Kasım 2017 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 24 Şubat 2022.
- "Merk". 26 Ağustos 2006 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 30 Ağustos 2006.
- "Pfizer Güney Afrika'ya Flukonazol Bağışlayacak". 24 Ekim 2010 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 30 Ağustos 2006.
- "Kurumsal Sorumluluk: Novartis". novartis.com. 1 Eylül 2017 tarihinde orijinalinden arşivlenmiştir. Erişim tarihi: 19 Mayıs 2016.




